
常温下,将等体积,等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7。下列关于滤液中的离子浓度关系不正确的是( )
A.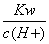 <1.0×10-7mol/L
<1.0×10-7mol/L
B.c(Na+)= c(HCO3-)+ c(CO32-)+ c(H2CO3)
C.c(H+)+c(NH4+)= c(OH-)+ c(HCO3-)+2 c(CO32-)
D.c(Cl-)> c(NH4+)> c(HCO3-)> c(CO32-)
【答案】C
【解析】A、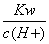 =c(OH-),pH<7时,c(OH-) 1.0×10-7mol/L ,A正确;B、物料守恒,B正确;C、电荷守恒,应为c(H+)+c(NH4+)= c(OH-)+ c(HCO3-)+2 c(CO32-)+ c(Cl-),C错误;D、c(Cl-)不变,NH4+水解,则c(Cl-)> c(NH4+),HCO3-部分结晶析出,则c(NH4+)> c(HCO3-),CO32-是HCO3-电离产生的,电离很微弱,则c(HCO3-)> c(CO32-),D正确。选C。
=c(OH-),pH<7时,c(OH-) 1.0×10-7mol/L ,A正确;B、物料守恒,B正确;C、电荷守恒,应为c(H+)+c(NH4+)= c(OH-)+ c(HCO3-)+2 c(CO32-)+ c(Cl-),C错误;D、c(Cl-)不变,NH4+水解,则c(Cl-)> c(NH4+),HCO3-部分结晶析出,则c(NH4+)> c(HCO3-),CO32-是HCO3-电离产生的,电离很微弱,则c(HCO3-)> c(CO32-),D正确。选C。
【考点定位】电解质溶液
【名师点睛】电解质溶液中离子浓度大小比较问题,是高考热点中的热点。多年以来全国高考化学试卷几乎年年涉及。这种题型考查的知识点多,灵活性、综合性较强,有较好的区分度,它能有效地测试出学生对强弱电解质、电离平衡、水的电离、pH、离子反应、盐类水解等基本概念的掌握程度以及对这些知识的综合运用能力。围绕盐类水解的类型和规律的应用试题在高考中常有涉及。考查的重点内容有:1、弱电解质的电离平衡(主要考查:电解质、非电解质的判断;某些物质的导电能力大小比较;外界条件对电离平衡的影响及电离平衡的移动;将电离平衡理论用于解释某些化学问题;同浓度(或同pH)强、弱电解质溶液的比较等等。);2、水的电离程度影响的定性判断与定量计算;3、盐溶液蒸干灼烧后产物的判断;4、溶液中离子浓度大小的比较等。


科目:高中化学 来源: 题型:
A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,A是地壳中含量最高的元素,B、C、D同周期,E和其他元素既不在同周期也不在同主族,D的氢化物和最高价氧化物对应的水化物均为强酸,且B、C、D的最高价氧化物对应的水化物两两混合均能发生反应生成盐和水。据此回答下列问题:
(1)A和D的氢化物中,沸点较低的是________(选“A”或“D”)。
(2)元素C在元素周期表中的位置是________,B的最高价氧化物对应的水化物的电子式为________。
(3)A、D、E可以形成多种盐,其中一种盐中A、D、E三种元素的原子个数比为2∶2∶1,该盐的名称为________。它的水溶液与D的氢化物的水溶液反应可生成D的单质,该反应的离子方程式为__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知α氨基酸与亚硝酸(HNO2)反应生成α羟基酸。如:
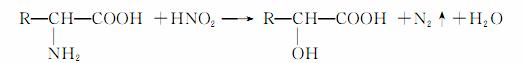 试根据下列6种有机物之间的转化关系,回答有关问题:
试根据下列6种有机物之间的转化关系,回答有关问题:
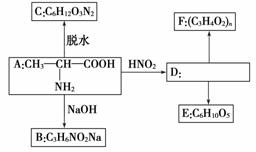
(1)写出有机物B和E的结构简式。
B:____________________,E:____________________。
(2)写出下列反应的化学方程式。
①A→C:________________________________________________________________________。
②D→F:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物M的结构简式如右图,下列说法正确的是
A.M在FeBr3 作催化剂时可与溴水发生取代反应
B.M与浓硫酸共热可发生消去反应
C.1molM发生消去反应时可消耗2molNaOH
D.M可发生消去、加成、取代、氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
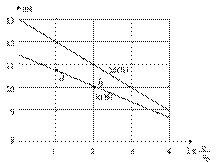 浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随
浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随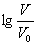 的变化如图所示,下列叙述错误的是( )
的变化如图所示,下列叙述错误的是( )
A.MOH的碱性强于ROH的碱性
B.ROH的电离程度:b点大于a点
C.若两溶液无限稀释,则它们的c(OH-)相等
D.当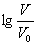 =2时,若两溶液同时升高温度,则
=2时,若两溶液同时升高温度,则 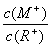 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
10ml浓度为1mol/L的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应速率但又不影响氢气生成的是( )
A.K2SO4 B.CH3COONa C.CuSO4 D.Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
研究硫元素及其化合物的性质具有重要意义。
(1)①硫离子的结构示意图为 。
②加热时,硫元素的最高价氧化物对应水化物的浓溶液与木炭反应的化学方程式为 ______ 。
(2)25℃,在0.10mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-) 关系如右图(忽略溶液体积的变化、H2S的挥发)。
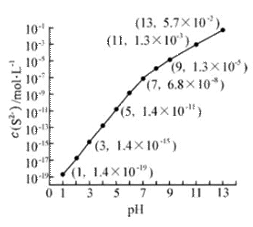
①pH=13时,溶液中的c(H2S)+c(HS-)= mol·L-1.
②某溶液含0.020 mol·L-1Mn2+、0.10 mol·L-1H2S,当溶液pH= 时,Mn2+开始沉淀。[已知:Ksp(MnS)=2.8×10-13]
(3) 25℃,两种酸的电离平衡常数如右表。
| Ka1 | Ka2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-4 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
①HSO3-的电离平衡常数表达式K= 。
②0.10 mol·L-1Na2SO3溶液中离子浓度由大到小的顺序为 。
③H2SO3溶液和NaHCO3溶液反应的主要离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
合金贮氢材料具有优异的吸收氢性能,在配合氢能的开发中起到重要作用。
(1)一定温度下,某贮氢合金(M)的贮氢过程如图所示,纵轴为平衡时氢气的压强(p),横轴表示固相中氢原子与金属原子的个数比(H/M)。
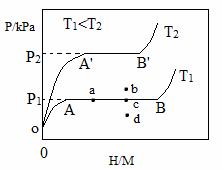
在OA段,氢溶解于M中形成固溶体MHx,随着氢气压强的增大,H/M逐惭增大;在AB段,MHx与氢气发生氢化反应生成氢化物MHy,氢化反应方程式为:zMHx(s)+H2(g)==ZMHy(s) △H(Ⅰ);在B点,氢化反应结束,进一步增大氢气压强,H/M几乎不变。反应(Ⅰ)中z=_____(用含x和y的代数式表示)。温度为T1时,2g某合金4min内吸收氢气240mL,吸氢速率v=______mL•g-1•min。反应的焓变△HⅠ_____0(填“>”“<”或“=”)。
(2)η表示单位质量贮氢合金在氢化反应阶段的最大吸氢量占其总吸氢量的比例,则温度为T1、T2时,η(T1)____η(T2)(填“>”“<”或“=”)。当反应(Ⅰ)处于图中a点时,保持温度不变,向恒容体系中通入少量氢气,达到平衡后反应(Ⅰ)可能处于图中的_____点(填“b”“c”或“d”),该贮氢合金可通过______或_______的方式释放氢气。
(3)贮氢合金ThNi5可催化由CO、H2合成CH4的反应,温度为T时,该反应的热化学方程式为_________。已知温度为T时:CH4(g)+2H2O=CO2(g)+4H2(g) △H=+165KJ•mol
CO(g)+H2O(g)=CO2(g)+H2(g) △H=-41KJ•mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.化学变化过程是原子的重新组合过程
B.化学反应的焓变用ΔH表示,单位是kJ·mol-1
C.化学反应的焓变ΔH越大,表示放热越多
D.化学反应中的能量变化不都是以热能形式表现出来的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com