
(����8��)��1����һ��������ܱ������У��������»�ѧ��Ӧ��
![]() A(g) + 3B(g) 2C(g) + D��s�� ��H���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
A(g) + 3B(g) 2C(g) + D��s�� ��H���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t/K | 298 | 398 | 498 | �� |
K/(mol?L��1)-2 | 4.1��106 | 8.2��107 | K1 | �� |
������������⣺
�� �÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK= ��
�� �жϸ÷�Ӧ�Ħ�H 0���>����<����
�� ��һ�������£������жϸ÷�Ӧ�Ѵﻯѧƽ��״̬���� ������ţ���
A��3v(B)������=2v(C)������ B��D�����ʵ�������
C��������ѹǿ���ֲ��� D�����������ܶȱ��ֲ���
��398K��1.01��105Pa��1L���ܱ������м���1molA��3molB����ƽ��ʱA��ת����Ϊa������ͬ�����µ���1L�����У���Ҫ�ﵽ��ǰһ��������ͬ������Ũ�ȣ�������� molC,D��ȡֵ��ΧΪ mol��
��2�������£�N2H6Cl2����һ����Ҫ�Ļ���ԭ�ϣ��������ӻ����������ˮ����Һ�����ԣ�ˮ��ԭ����NH4Cl���ơ�
��д�������µ�һ��ˮ�ⷴӦ�����ӷ���ʽ ��
��������ˮ��Һ������Ũ�ȵ�����˳����ȷ���� ������ţ���
A��c(Cl��) > c(N2H62+) > c(H+) > c(OH��)
B��c(Cl��) > c(H+)> c([N2H5?H2O] +) > c(OH��)
C��2 c(N2H62+)+ c([N2H5?H2O] +)+c(H+)= c(Cl-)+c(OH��)
D��c(N2H62+) > c(Cl��) > c(H+) > c(OH��)
 Сѧ�̲�ȫ��ϵ�д�
Сѧ�̲�ȫ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��09��10ѧ�꽭����Ǩ��ѧ��һ��ѧ�����п��Ի�ѧ�� ���ͣ������
������8�֣���״����6.72L������������������ȫȼ�ա���������ͨ����������ʯ��ˮ�У��õ���ɫ��������Ϊ60.0g�����������ļ�ʯ������ȼ�ղ����ʯ������42.6g��
��1������ȼ�ղ�����ˮ����������2��ͨ�������ƶ����ķ���ʽ����3��д��һ�ֺ���������̼ͬԭ�Ӻ���ԭ���������ĺ���������Ľṹ��ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ���㽭ʡͩ���и�����ѧ��10�·��¿���ѧ�Ծ� ���ͣ�ʵ����
������8�֣���ͼ��ʾ�����ס�������װ�в�ͬ���ʵ���Ͳ�õ�������������������Ͳ�ڵ�����ѹ������Ͳ�ڣ������±����еIJ���ʵ�飨������ͬ��ͬѹ�²ⶨ����
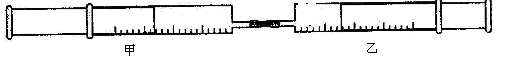
�Իش��������⣺

��1��ʵ��1�У��������ձ�Ϊ�� ɫ��д��������ɫ�Ļ�ѧ����ʽ ��
��2��ʵ��2�У���֪��3Cl2+2NH3=N2+6HCl������Ͳ���������ƶ�, ��Ͳ���а��̲����⣬�������ɫ�仯Ϊ �����������Ͳ�й�ʣ����������ԼΪ mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������8�֣���״����6.72L������������������ȫȼ�ա���������ͨ����������ʯ��ˮ�У��õ���ɫ��������Ϊ60.0g�����������ļ�ʯ������ȼ�ղ����ʯ������42.6g��
��1������ȼ�ղ�����ˮ����������2��ͨ�������ƶ����ķ���ʽ����3��д��һ�ֺ���������̼ͬԭ�Ӻ���ԭ���������ĺ���������Ľṹ��ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������8�֣���ͼ��ʾ�����ס�������װ�в�ͬ���ʵ���Ͳ�õ�������������������Ͳ�ڵ�����ѹ������Ͳ�ڣ������±����еIJ���ʵ�飨������ͬ��ͬѹ�²ⶨ����
�Իش��������⣺
��1��ʵ��1�У��������ձ�Ϊ�� ɫ��д��������ɫ�Ļ�ѧ����ʽ ��
��2��ʵ��2�У���֪��3Cl2+2NH3=N2+6HCl������Ͳ���������ƶ�, ��Ͳ���а��̲����⣬�������ɫ�仯Ϊ �����������Ͳ�й�ʣ����������ԼΪ mL��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com