
¹żŃõ»ÆĒā£ØH2O2£¬OµÄ»ÆŗĻ¼ŪĪŖ£1¼Ū£©Ė׳ĘĖ«ŃõĖ®£¬Ņ½ĮĘÉĻĄūÓĆĖüӊɱ¾śĻū¶¾×÷ÓĆĄ“ĒåĻ“ÉĖæŚ”£ŃŠ¾æĻĀĮŠÉę¼°H2O2µÄ·“Ó¦£¬Ķź³ÉĻĀĮŠø÷Ģā£ŗ
A£®Ag2O+ H2O2£½2Ag+O2 ”ü+ H2O
B£®3H2O2+Cr2(SO4)3+10KOH£½2K2CrO4+3K2SO4+8H2O
£Ø1£©Š“³öŅ»øöH2O2¼ČĢåĻÖŃõ»ÆŠŌÓÖĢåĻÖ»¹ŌŠŌµÄ»Æѧ·“Ó¦·½³ĢŹ½ ”£
£Ø2£©½«ĻĀĮŠĪļÖŹ£ŗH2O2”¢K2SO4”¢MnSO4”¢H2SO4”¢KMnO4”¢O2µÄ»ÆѧŹ½·Ö±šĢīŌŚæհד¦×é³ÉŅ»øö²»ŠčÅäĘ½µÄ»Æѧ·½³ĢŹ½£ŗ + +______ ”ś + + + H2O
¢ŁøĆ·“Ó¦ÖŠµÄ»¹Ō¼ĮŹĒ ”£
¢ŚøĆ·“Ó¦ÖŠ£¬·¢Éś»¹Ō·“Ó¦µÄŌŖĖŲŹĒ ”£
£Ø3£©Ńõ»ÆŠŌ£ŗKMnO4_____K2CrO4£ØĢī”°£¾”±»ņ”°£¼”±£©”£
£Ø1£©2H2O2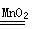 2H2O + O2”ü £Ø2£©H2O2+KMnO4+H2SO4”śMnSO4+O2+K2SO4+ H2O
2H2O + O2”ü £Ø2£©H2O2+KMnO4+H2SO4”śMnSO4+O2+K2SO4+ H2O
¢ŁH2O2 ¢ŚMn £Ø3£©£¾
½āĪöŹŌĢā·ÖĪö£ŗ£Ø1£©H2O2¼ČĢåĻÖŃõ»ÆŠŌÓÖĢåĻÖ»¹ŌŠŌ£¬ÕāĖµĆ÷øĆ·“Ó¦Ņ»¶ØŹĒĖ«ŃõĖ®µÄ·Ö½ā·“Ó¦£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ2H2O2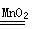 2H2O + O2”ü”£
2H2O + O2ӟӣ
£Ø2£©øßĆĢĖį¼Ų¾ßÓŠĒæŃõ»ÆŠŌ£¬ĘäŃõ»ÆŠŌĒæÓŚĖ«ŃõĖ®µÄ£¬ĖłŅŌøßĆĢĖį¼ŲÄÜ°ŃĖ«ŃõĖ®Ńõ»ÆÉś³ÉŃõĘų£¬¶ųøßĆĢĖį¼ŲµÄ»¹Ō²śĪļŹĒĮņĖįĆĢ£¬Ņņ“ĖøĆ·“Ó¦µÄ·½³ĢŹ½æÉŅŌ±ķŹ¾ĪŖH2O2+KMnO4+H2SO4”śMnSO4+O2+K2SO4+ H2O”£
¢ŁĖ«ŃõĖ®ÖŠŃõŌŖĖŲµÄ»ÆŗĻ¼Ū“Ó£1¼ŪÉżøßµ½0¼Ū£¬±»Ńõ»Æ£¬Ņņ“ĖĖ«ŃõĖ®ŹĒ»¹Ō¼Į”£
¢ŚøßĆĢĖį¼ŲÖŠMnŌŖĖŲµÄ»ÆŗĻ¼Ū“Ó£«7¼Ū½µµĶµ½£«2¼Ū£¬µĆµ½µē×Ó£¬±»»¹Ō£¬ĖłŅŌ±»»¹ŌµÄŌŖĖŲŹĒMn”£
£Ø3£©ŌŚ·“Ó¦3H2O2+Cr2(SO4)3+10KOH£½2K2CrO4+3K2SO4+8H2OÖŠ£¬Ė«ŃõĖ®ŹĒŃõ»Æ¼Į£¬K2CrO4ŹĒŃõ»Æ²śĪļ£¬Ōņøł¾ŻŃõ»Æ¼ĮµÄŃõ»ÆŠŌĒæÓŚŃõ»Æ²śĪļµÄæÉÖŖ£¬Ńõ»ÆŠŌŹĒĖ«ŃõĖ®ĒæÓŚK2CrO4£»ŌŚ·“Ó¦H2O2+KMnO4+H2SO4”śMnSO4+O2+K2SO4+ H2OÖŠ£¬øßĆĢĖį¼ŲŹĒŃõ»Æ¼Į£¬ĘäŃõ»ÆŠŌĒæÓŚĖ«ŃõĖ®µÄ£¬ĖłŅŌøßĆĢĖį¼ŲµÄŃõ»ÆŠŌĒæÓŚK2CrO4”£
æ¼µć£ŗæ¼²éŃõ»Æ»¹Ō·“Ó¦µÄÓ¦ÓĆ”¢ÅŠ¶Ļ


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
µŖŌŖĖŲµÄ»ÆŗĻĪļŌŚ¹¤Å©ŅµŅŌ¼°¹ś·ĄæĘ¼¼ÖŠÓĆĶ¾¹ć·ŗ£¬µ«Ņ²»į¶Ō»·¾³Ōģ³ÉĪŪČ¾£¬ČēµŲĻĀĖ®ÖŠĻõĖįŃĪŌģ³ÉµÄµŖĪŪČ¾ŅŃ³ÉĪŖŅ»øöŹĄ½ēŠŌµÄ»·¾³ĪŹĢā”£
Ķź³ÉĻĀĮŠĢīæÕ£ŗ
£Ø1£©Ä³æĪĢā×éÄ£ÄāµŲĻĀĖ®ĶѵŖ¹ż³Ģ£¬ĄūÓĆFe·ŪŗĶKNO3(aq)·“Ó¦Ģ½¾æĶѵŖŌĄķ”£ŹµŃéĒ°
¢ŁÓĆ0.1mol”¤L-1H2SO4(aq)Ļ“µÓFe·Ū£¬ĘäÄæµÄŹĒ £¬Č»ŗóÓĆÕōĮóĖ®Ļ“µÓÖĮÖŠŠŌ£»
¢Ś½«KNO3(aq)µÄpHµ÷ÖĮ2.5£»
¢ŪĪŖ·ĄÖ¹æÕĘųÖŠµÄ £ØŠ“»ÆѧŹ½£©¶ŌĶѵŖµÄÓ°Ļģ£¬Ó¦ĻņKNO3ČÜŅŗÖŠĶØČėN2”£
£Ø2£©ÓĆ×ćĮæFe·Ū»¹ŌÉĻŹöKNO3(aq)¹ż³ĢÖŠ£¬·“Ó¦ĪļÓėÉś³ÉĪļµÄĄė×ÓÅØ¶Č”¢pHĖꏱ¼äµÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾”£Ēėøł¾ŻĶ¼ÖŠŠÅĻ¢Š“³öt1Ź±æĢĒ°øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ ”£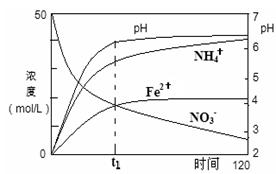
£Ø3£©ÉńÖŪŌŲČĖ·É“¬µÄ»š¼żĶĘ½ųĘ÷ÖŠ³£ÓĆėĀ£ØN2H4£©×÷Č¼ĮĻ”£NH3ÓėNaClO·“Ó¦æɵƵ½ėĀ£ØN2H4£©£¬øĆ·“Ó¦ÖŠ±»Ńõ»ÆÓė±»»¹ŌµÄŌŖĖŲµÄŌ×ÓøöŹżÖ®±ČĪŖ ”£Čē¹ū·“Ó¦ÖŠÓŠ5molµē×Ó·¢Éś×ŖŅĘ£¬æɵƵ½ėĀ g”£
£Ø4£©³£ĪĀĻĀĻņ25mL 0.01mol/LĻ”ŃĪĖįÖŠ»ŗ»ŗĶØČė5.6 mL NH3£Ø±ź×¼×“æö£¬ČÜŅŗĢå»ż±ä»ÆŗöĀŌ²»¼Ę£©£¬·“Ó¦ŗóČÜŅŗÖŠĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņŹĒ ”£ŌŚĶØČėNH3µÄ¹ż³ĢÖŠČÜŅŗµÄµ¼µēÄÜĮ¦ £ØĢīŠ“”°±ä“ó”±”¢”°±äŠ””±»ņ”°¼øŗõ²»±ä”±£©”£
£Ø5£©ĻņÉĻŹöČÜŅŗÖŠ¼ĢŠųĶØČėNH3£¬øĆ¹ż³ĢÖŠĄė×ÓÅØ¶Č“óŠ”¹ŲĻµæÉÄÜÕżČ·µÄŹĒ £ØŃ”Ģī±ąŗÅ£©”£
a£®c(Cl-)=c(NH4+)£¾c(H+)=c(OH-) b£®c(Cl-)£¾c(NH4+)=c(H+)£¾c(OH-)
c£®c(NH4+)£¾c(OH-)£¾c(Cl-)£¾c(H+) d£®c(OH-)£¾c(NH4+)£¾c(H+)£¾c(Cl-)
£Ø6£©³£ĪĀĻĀĻņ25mLŗ¬HCl 0.01molµÄČÜŅŗÖŠµĪ¼Ó°±Ė®ÖĮ¹żĮ棬øĆ¹ż³ĢÖŠĖ®µÄµēĄėĘ½ŗā £ØĢīŠ“µēĄėĘ½ŗāŅʶÆĒéæö£©”£µ±µĪ¼Ó°±Ė®µ½25mLŹ±£¬²āµĆČÜŅŗÖŠĖ®µÄµēĄė¶Č×ī“ó£¬Ōņ°±Ė®µÄÅضČĪŖ mol”¤L-1”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
Ńõ»Æ»¹Ō·“Ó¦ŌŚÉś²ś”¢Éś»īÖŠ¾ßÓŠ¹ć·ŗµÄÓĆĶ¾£¬¹į“©¹Å½ń”£
£Ø1£©ĻĀĮŠÉś²ś”¢Éś»īµÄŹĀĄżÖŠ·¢ÉśĮĖŃõ»Æ»¹Ō·“Ó¦µÄŹĒ ”£
£Ø2£©Ė®ŹĒČĖĢåµÄÖŲŅŖ×é³É²æ·Ö£¬ŹĒČĖĢåÖŠŗ¬Įæ×ī¶ąµÄŅ»ÖÖĪļÖŹ”£¶ų”°ĖÄÖÖ»ł±¾·“Ó¦ĄąŠĶÓėŃõ»Æ»¹Ō·“Ó¦µÄ¹ŲĻµ”±Ņ²æÉÓĆČēĶ¼±ķ“ļ”£
ŹŌŠ“³öÓŠĖ®²Ī¼Ó”¢Ė®ĪŖ»¹Ō¼ĮĒŅĪŖĄąŠĶ¢ōµÄŅ»øö»Æѧ·½³ĢŹ½£ŗ ”£
£Ø3£©NaNO2ŹĒŅ»ÖÖŹ³Ę·Ģķ¼Ó¼Į£¬ĖüÄÜÖĀ°©”£ĖįŠŌKMnO4ČÜŅŗÓėNaNO2·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ£ŗ
¢ŁĒė²¹³äĶźÕū£¬ÅäĘ½·½³ĢŹ½²¢±ź³öµē×Ó×ŖŅʵķ½ĻņŗĶŹżÄ攣
¢ŚÄ³Ķ¬Ń§³ĘČ”ĮĖ7.9 g KMnO4£¬¹ĢĢ壬ÓūÅäÖĘ100 mLČÜŅŗ”£»Ų“šĻĀĮŠĪŹĢā£ŗ
øĆŹµŃéÖŠ£¬Ź¹ÓĆČŻĮæĘæŹ±ŅŖ¼ģ²éŹĒ·ńĀ©Ė®£¬Ęä²Ł×÷ŹĒ ”£
¢Ū²»¹ę·¶µÄŹµŃé²Ł×÷»įµ¼ÖĀŹµŃé½į¹ūµÄĪó²ī”£ĻĀĮŠ²Ł×÷»įŹ¹ŹµŃé½į¹ūĘ«Š”µÄŹĒ (ĢīŠņŗÅ)”£
A£®ŌŚČܽā¹ż³ĢÖŠÓŠÉŁĮæŅŗĢ彦³öÉÕ±Ķā
B£®¶ØČŻŹ±ŃöŹÓČŻĮæĘæÉĻµÄæĢ¶ČĻß
C£®¶ØČŻŗ󣬽«ČŻĮæĘæÕńµ“Ņ”ŌČŗ󣬾²ÖĆ·¢ĻÖŅŗĆęµĶÓŚæĢ¶ČĻߣ¬ÓŚŹĒÓÖ¼ÓČėÉŁĮæĖ®ÖĮæĢ¶ČĻß
¢ÜijĶ¬Ń§ÓĆÉĻŹöÅäŗƵÄKMnO4ČÜŅŗµĪ¶ØĪ“ÖŖÅØ¶ČµÄNaNO2ČÜŅŗ£ŗČ”20 mLĪ“ÖŖÅØ¶ČµÄNaNO2ČÜŅŗӌ׶ŠĪĘæ£»Č”ÉĻŹöÅäŗƵÄKMnO4ČÜŅŗÓŚ________(Ģī”°ĖįŹ½”±»ņ”°¼īŹ½”±)µĪ¶Ø¹Ü£¬µĪ¶ØĶź³ÉŗóĻūŗÄKMnO4ČÜŅŗ10 mL£¬ŌņNaNO2ČÜŅŗµÄÅضČĪŖ________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
³£ĪĀĻĀKMnO4Ńõ»ÆÅØHClµÄ·“Ó¦·½³ĢŹ½ČēĻĀ£ŗ2KMnO4 £«16HCl£ØÅØ£©=2KCl£«2MnCl 2£«5Cl 2”ü£«8H2O
£Ø1£©ÓĆ”°Ė«ĻßĒÅ·Ø”±±źĆ÷·“Ó¦ÖŠµē×Ó×ŖŅʵķ½ĻņŗĶŹżÄ攣
£Ø2£©ÓÖŅŃÖŖ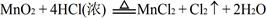 £¬½įŗĻŅŌÉĻ·“Ó¦ŌĄķ£¬ŌņMnO2”¢KMnO4”¢Cl2µÄŃõ»ÆŠŌÓÉĒæµ½ČõµÄĖ³ŠņŹĒ£ŗ ”£
£¬½įŗĻŅŌÉĻ·“Ó¦ŌĄķ£¬ŌņMnO2”¢KMnO4”¢Cl2µÄŃõ»ÆŠŌÓÉĒæµ½ČõµÄĖ³ŠņŹĒ£ŗ ”£
£Ø3£©ČōÓŠ63.2gøßĆĢĖį¼Ų²Ī¼Ó·“Ó¦£¬Ōņ±»Ńõ»ÆµÄHClµÄĪļÖŹµÄĮæĪŖ mol£¬²śÉśµÄCl2ŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ L”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
¢ń£®ĻÖÓŠ°ĖÖÖĪ¢Į££ŗNa”¢Mg2+”¢Fe2+”¢Fe3+”¢S2-”¢SO2”¢HCl”¢H2O£¬“ÓŌŖĖŲ»ÆŗĻ¼ŪµÄ½Ē¶Č·ÖĪö£¬ĘäÖŠÖ»ÓŠŃõ»ÆŠŌµÄŹĒ______ £¬Ö»ÓŠ»¹ŌŠŌµÄŹĒ_____ _£¬
¼ČÓŠŃõ»ÆŠŌÓÖÓŠ»¹ŌŠŌµÄŹĒ__________ _”£
¢ņ£®ŅŃÖŖÄÜÓĆĀČĖį¼ŲÓėÅØŃĪĖį·“Ó¦ÖĘČ”ĀČĘų£¬Ęä»Æѧ·½³ĢŹ½ČēĻĀ£ŗ
KClO3+6HCl=KCl+3Cl2ӟ+ 3H2O
¢ÅÓƵ„ĻßĒÅŌŚÉĻŹö·½³ĢŹ½ÖŠ±ź³öµē×Ó×ŖŅʵķ½ĻņŗĶŹżÄ攣
¢Ę±źæöĻĀÉś³É3£®36LCl2£¬×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ £¬±»Ńõ»ÆµÄŃĪĖįÓėĪ“±»Ńõ»ÆµÄŃĪĖįÖŹĮæÖ®±ČĪŖ ”£Ńõ»Æ²śĪļÓė»¹Ō²śĪļĪļÖŹµÄĮæÖ®±ČĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
£Ø1£©ČēĶ¼ŹĒæĪ±¾ÖŠ”°ĖÄÖÖ»ł±¾·“Ó¦ĄąŠĶÓėŃõ»Æ»¹Ō·“Ó¦µÄ¹ŲĻµ”±Ķ¼£¬”°H2+CuO  Cu+H2O”±·“Ó¦ŹōÓŚĶ¼ÖŠµÄĒųÓņ £ØĢīŠņŗÅ£©”£ĻĀĮŠ·“Ó¦ÖŠŹōÓŚĒųÓņ7µÄÓŠ ”£
Cu+H2O”±·“Ó¦ŹōÓŚĶ¼ÖŠµÄĒųÓņ £ØĢīŠņŗÅ£©”£ĻĀĮŠ·“Ó¦ÖŠŹōÓŚĒųÓņ7µÄÓŠ ”£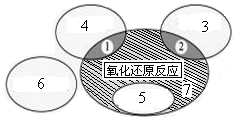
A£®2H2+O2 2H2O 2H2O |
B£®2NaHCO3 Na2CO3+H2O+CO2”ü Na2CO3+H2O+CO2”ü |
| C£®Zn+H2SO4=ZnSO4+H2”ü |
D£®CuO+CO Cu+CO2 Cu+CO2 |
 N2+6NH4Cl
N2+6NH4Cl²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
Ķعż¶ŌÄ£ŠĶ”¢Ķ¼ŠĪ”¢Ķ¼±ķµÄ¹Ū²ģ£¬ÄÜ»ńȔӊ¹ŲŠÅĻ¢ŹĒ»ÆѧѧĻ°µÄŅ»ÖÖÖŲŅŖÄÜĮ¦”£°“ŅŖĒó»Ų“šĻĀĮŠĪŹĢā”£
(1) ĻÖÓŠĻĀĮŠ¶ĢÖÜĘŚŌŖĖŲŠŌÖŹµÄ²æ·ÖŹż¾Ż£¬ĘäÖŠXŹżÖµŹĒ±ķŹ¾²»Ķ¬ŌŖĖŲµÄŌ×ÓŌŚ·Ö×ÓÄŚĪüŅżµē×ÓµÄÄÜĮ¦“󊔣¬ČōXÖµŌ½“ó£¬ĘäŌ×ÓĪüŅżµē×ÓÄÜĮ¦Ō½Ē棬ŌŚĖłŠĪ³ÉµÄ·Ö×ÓÖŠ³ÉĪŖ“ųøŗµēŗÉŅ»·½£ŗ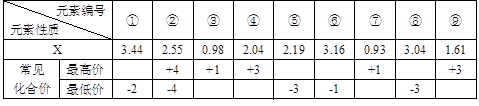
Š“³öĻĀĮŠ±ąŗÅĖł“ś±ķµÄŌŖĖŲ·ūŗÅ£ŗ¢Ł____£¬¢Ś____£¬¢Ü____£¬¢Ż____£¬¢Ž____”£
(2) ŅŃÖŖ4ÖÖĪŽ»ś»ÆŗĻĪļŌŚĖ®ÖŠŗĶŅŗ°±ÖŠµÄČܽā¶Č(g/100gČܼĮ)ĪŖ£ŗ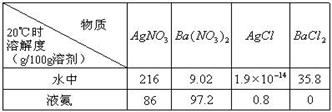
ÓÉÉĻ±ķµÄŹż¾ŻæÉÖŖ£¬ŌŚĖ®ČÜŅŗÖŠÉĻŹö»ÆŗĻĪļ·¢Éśø“·Ö½ā·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ______________________£¬ŌŚŅŗ°±ČÜŅŗÖŠ·¢Éśø“·Ö½ā·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ______________________________________________”£
(3) ijĻ”ČÜŅŗÖŠŗ¬ÓŠFe(NO3)3”¢Cu(NO3)2”¢HNO3£¬ĻņĘäÖŠÖš½„¼ÓČėĢś·Ū£¬ČÜŅŗÖŠFe2+µÄÅضČŗĶ¼ÓČėĢś·ŪµÄĪļÖŹµÄĮæÖ®¼äµÄ¹ŲĻµČēÓŅĶ¼ĖłŹ¾”£ČżÖÖĪļÖŹŗĶĢś·¢Éś·“Ó¦µÄĖ³ŠņĪŖ___________£¬µŚŅ»²½·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ________£¬ÓÉĶ¼æÉÖŖČÜŅŗÖŠFe(NO3)3”¢Cu(NO3)2”¢HNO3ĪļÖŹµÄĮæÅضČÖ®±ČĪŖ__________”£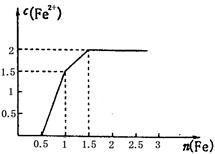
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
¢ń.Ā±»ÆĪļŗĶĀ±ĖįŃĪŌŚ¹¤ŅµÉś²śÖŠÓŠ×ÅÖŲŅŖµÄ×÷ÓĆ”£Ä³Š”×éĪŖĢ½¾æĘäÖŠŅ»Š©ŃĪµÄŠŌ
ÖŹ£¬²éŌÄ׏ĮĻ²¢½ųŠŠŹµŃ锣²éŌÄ׏ĮĻČēĻĀ£ŗ
¢Ł BrO3£ + 6I£ + 6H+ = 3I2 + Br£+ 3H2O ¢Ś 2BrO3£ + I2 = 2IO3£ + Br2
¢Ū IO3£ + 5I£ + 6H+ = 3I2 + 3H2O ¢Ü 2IO3£ + 10Br£+ 12H+ = I2 + 5Br2 + 6H2O
ŹµŃéČēĻĀ£ŗ
| ²½Öč | ĻÖĻó |
| ¢”.ĻņŹ¢ÓŠ30 mL 0.2 mol”¤L-1 KIČÜŅŗµÄ׶ŠĪĘæÖŠŅĄ“ĪµĪČė¼øµĪµķ·ŪČÜŅŗŗĶ×ćĮæĻ”ĮņĖį£¬ŌŁÓƵĪ¶Ø¹ÜÖšµĪ¼ÓČėKBrO3ČÜŅŗ | Ėę×ÅKBrO3ČÜŅŗµĪČė£¬ČÜŅŗÓÉĪŽÉ«±äĪŖĄ¶É«²¢Öš½„¼ÓÉī,×īÖÕ±£³Ö²»±ä |
| ¢¢.¼ĢŠųĻņÉĻŹöČÜŅŗÖŠµĪČėKBrO3ČÜŅŗ | ČÜŅŗµÄĄ¶É«Öš½„ĶŹČ„ |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
ŌŚ50 mL a mol”¤L-1µÄĻõĖįČÜŅŗÖŠ£¬¼ÓČė6£®4g Cu£¬Č«²æČܽā£¬¼ŁÉčĻõĖįµÄ»¹Ō²śĪļÖ»ÓŠNO2ŗĶNO£¬½«·“Ó¦ŗóČÜŅŗÓĆÕōĮóĖ®Ļ”ŹĶÖĮ100 mLŹ±²āµĆc(NO3-)£½3 mol”¤L-1”£
(1)ĒóĻ”ŹĶŗóµÄČÜŅŗÖŠH+µÄĪļÖŹµÄĮæÅضČ
(2)Čōa£½9£¬ĒóÉś³ÉµÄĘųĢåÖŠNO2µÄĪļÖŹµÄĮæ
(3)ÖĪĄķµŖŃõ»ÆĪļĪŪČ¾µÄ·½·ØÖ®Ņ»ŹĒÓĆNaOHČÜŅŗ½ųŠŠĪüŹÕ£¬·“Ó¦ŌĄķČēĻĀ£ŗ
NO2£«NO£«2NaOH£½2NaNO2£«H2O”¢2NO2£«2NaOH£½NaNO2£«NaNO3£«H2O”£Čō½«ÉĻŹöµÄNO2ŗĶNOµÄ»ģŗĻĘųĢåĶØČė1 mol”¤L-1µÄNaOHČÜŅŗĒ”ŗƱ»ĪüŹÕ£¬ĒóŠčŅŖNaOHČÜŅŗµÄĢå»ż”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com