
短周期元素X、Y、Z、W、Q在元素周期表中的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法中正确的是双选) )。
A.钠与W可能形成Na2W2化合物
B.由Z与Y组成的物质在熔融时能导电
C.W得电子能力比Q弱
D.X有多种同素异形体,而Y不存在同素异形体
| X | Y | ||
| Z | W | Q |
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
下图曲线a表示放热反应X(g)+Y(g)Z(g)+M(g)+N(s)进行过程中,X的转化率随时间t变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采用的措施是( )

A.升高温度 B.加大X的投入量
C.加催化剂 D.增大体积
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.分散系中分散质粒子的直径:Fe(OH)3悬浊液> Fe(OH)3胶体> FeCl3溶液
B.能自发进行的化学反应,一定是 H<0、
H<0、 S>0
S>0
C.焰色反应是物质燃烧时火焰呈现的颜色变化,属于化学变化
D.钢铁发生电化学腐蚀时,负极的电极反应式为Fe-3e-= Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是某煤化工产业链的一部分,试运用所学知识,解决下列问题:
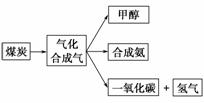
1)已知该产业链中某反应的平衡常数表达式为K=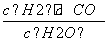 ,它所对应反应的化学方程式是
,它所对应反应的化学方程式是
____________________________________________________。
2)合成甲醇的主要反应是2H2g)+COg)CH3OHg) ΔH=-90.8 kJ·mol-1,t ℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应10 min后测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度mol·L-1) | 0.2 | 0.1 | 0.4 |
①该时间段内反应速率vH2)=________。
②比较此时正、逆反应速率的大小:v正________v逆填“>”、“<”或“=”)。
③反应达到平衡后,保持其他条件不变,若只把容器的体积缩小一半,平衡 ________填“逆向”、“正向”或“不”)移动,平衡常数K________填“增大”、“减小”或“不变”)。
3)固氮是科学家致力研究的重要课题。自然界中存在天然的大气固氮过程:
N2g)+O2g)===2NOg) ΔH=+180.8 kJ·mol-1,工业合成氨则是人工固氮。
分析两种固氮反应的平衡常数,下列结论正确的是________填字母序号)。
| 反应 | 大气固氮 | 工业固氮温度/℃ | ||||
| 27 | 2 000 | 25 | 350 | 400 | 450 | |
| K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.507 | 0.152 |
A.常温下,大气固氮很难进行,而工业固氮却能非常容易进行
B.模拟大气固氮应用于工业上的意义不大
C.工业固氮时温度越低,氮气与氢气反应越完全
D.K越大说明合成氨反应的速率越大
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在常温常压下:
①2CH3OHl)+3O2g)===2CO2g)+4H2Og)
ΔH1=-1 275.6 kJ·mol-1
②2COg)+O2g)===2CO2g)
ΔH2=-566.0 kJ·mol-1
③H2Og)===H2Ol) ΔH3=-44.0 kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:________________________________________________________
____________________________________________________。
2)H2或CO可以催化还原NO以达到消除污染的目的。
已知:N2g)+O2g)===2NOg)
ΔH=+180.5 kJ·mol-1
2H2g)+O2g)===2H2Ol)
ΔH=-571.6 kJ·mol-1
则H2g)与NOg)反应生成N2g)和H2Ol)的热化学方程式为________________________________________________________
____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据元素周期律判断,下列递变规律不正确的是 )。
A.Na、Mg、Al的金属性依次减弱
B.HCl、HBr、HI的稳定性依次增强
C.HClO4、H2SO4、H3PO4的酸性依次减弱
D.Li、Na、K与水反应的剧烈程度依次增大
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解200 mL一定浓度的硫酸铜溶液,实验装置如图①所示,电解过程中的实验数据如图②所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况)。

(1)下列说法正确的是______(填序号)。
A.电解过程中,b电极表面先有红色物质析出,后有气泡产生
B.a电极上发生的反应为2H++2e-===H2↑和4OH--4e-===2H2O+O2↑
C.从P点到Q点时收集到的混合气体的平均摩尔质量为12 g·mol-1
D.OP段表示H2和O2混合气体的体积变化,PQ段表示O2的体积变化
(2)如果要使溶液恢复到电解前的状态,向溶液中加入0.8 g CuO即可,则电解后溶液的pH为______。
(3)如果向所得的溶液中加入0.1 mol Cu(OH)2后,使溶液恰好恢复到电解前的浓度和pH,电解过程中转移的电子为______mol。
(4)如果向所得的溶液中加入0.1 mol Cu2(OH)2CO3后,使溶液恰好恢复到电解前的浓度和pH(不考虑CO2的溶解),电解过程中转移的电子为______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
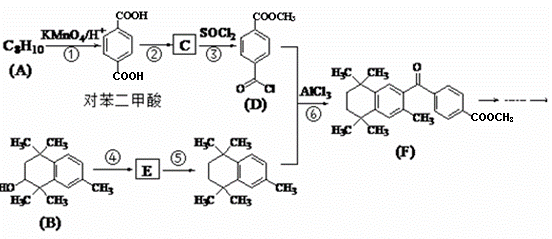 历史上曾将一类从植物胶中取得的具有芳香气味的物质称为芳香族化合物,芳香族化合物大部分具有“芳香性”,有研究者设计利用其特殊性质合成某药物,其合成路线如下(部分反应试剂和条件已略):
历史上曾将一类从植物胶中取得的具有芳香气味的物质称为芳香族化合物,芳香族化合物大部分具有“芳香性”,有研究者设计利用其特殊性质合成某药物,其合成路线如下(部分反应试剂和条件已略):
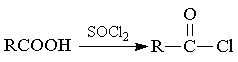
已知:Ⅰ. 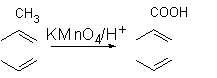
 Ⅱ.
Ⅱ.
试回答下列问题:
(1)原料A的结构简式为 ;原料B发生反应④所需的条件为 。
(2)D的分子式为 ;F分子中含氧官能团的名称为 、 。
(3)反应①、⑥所属的反应类型分别为 、 。
(4)反应②、⑤的化学方程式分别为②______________;⑤______________。
(5)对苯二甲酸有多种同分异构体,符合下列条件的同分异构体有 种,
①苯环上有三个取代基;②能与NaHCO3溶液发生反应;③能发生银镜反应。
写出其中一个同分异构体发生银镜反应并酸化以后的产物的核磁共振氢谱为四组峰,且峰面积比为1:2:2:1的同分异构体的结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验。
②将Cl2通入水中,所得溶液中具有氧化性的含氯粒子是________。
③设计实验比较Cl2和Br2的氧化性,操作与现象是:取少量新制氯水和CCl4于试管中,____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com