
【题目】在一定条件下,向![]() 和过量C粉的混合物中通入氯气,可制得易水解的
和过量C粉的混合物中通入氯气,可制得易水解的![]() ,实验装置如图所示。下列说法不正确的是
,实验装置如图所示。下列说法不正确的是 ![]()
![]()

A.c中盛装的是浓硫酸
B.实验结束时,应先熄灭d处酒精灯,待装置冷却后再熄灭a处酒精灯
C.此反应中的尾气除氯气外都可直接排放到大气中
D.该装置不完善,其中应改进的一项是在d、e之间添加一个干燥装置
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将装有甲烷和氯气混合气体的三个集气瓶,用玻璃片把瓶口盖好后,分别作如下处理,请回答下列问题。
(1)置于黑暗处,现象为___。
(2)将点燃的镁条靠近集气瓶外壁,产生的现象为___。
(3)放在光亮的教室里,产生的现象为___。
(4)甲烷和氯气发生的一系列反应都是___(填“取代”或“加成”)反应,该反应的有机产物中常用作有机溶剂的是___,可用作灭火剂的是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图中的实验方案,能达到实验目的是( )
A.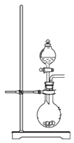 可用于制取少量NH3或用MnO2和浓盐酸制取Cl2
可用于制取少量NH3或用MnO2和浓盐酸制取Cl2
B. 可用于制取乙烯并检验乙烯
可用于制取乙烯并检验乙烯
C. 可以验证FeCl3对H2O2分解反应有催化作用
可以验证FeCl3对H2O2分解反应有催化作用
D. 先从
先从![]() 口进气集满CO2,再从
口进气集满CO2,再从![]() 口进气,可用于收集NO
口进气,可用于收集NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A(C12H16O2)具有芳香气味,常用作芳香剂。

已知:①B属于芳香族化合物且结构中只有一个侧链,分子式为C8Hl0O;
②D、E具有相同官能团,核磁共振氢谱测得E分子中有3种不同的峰。
回答下列问题:
(1)C可能发生的反应有___(填序号)。
①取代反应②消去反应③水解反应④加成反应
(2)与D属于同系物的同分异构体有___种(不包括D)。
(3)B发生消去反应所得有机物的结构简式为_____。
(4)B和E反应生成A的化学方程式为_______。
(5)C生成D的化学方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汞(熔点-39℃,沸点356℃)是制造电池、电极的重要原料,历史上曾用“灼烧辰砂法”制取汞。目前工业上制粗汞的一种流程图如下。
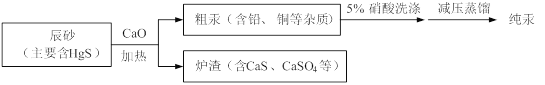
下列分析错误的是
A.洗涤粗汞可用5%的盐酸代替5%的硝酸
B.辰砂与氧化钙加热反应时,CaSO4为氧化产物
C.“灼烧辰砂法”过程中电子转移的方向和数目可表示为: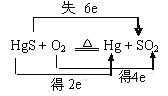
D.减压蒸馏的目的是降低汞的沸点,提高分离效率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置制取并收集气体,对应的装置和试剂均正确的是( )
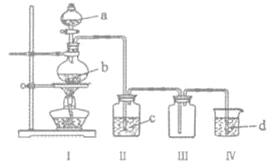
Ⅲ收集气体 | Ⅰ中试剂a,b | Ⅱ中试剂c | Ⅳ中试剂d | |
A | SO2 | 稀硫酸与铜片 | 浓硫酸 | NaOH溶液 |
B | Cl2 | 浓盐酸与二氧化锰 | 饱和氯化钠溶液 | NaOH 溶液 |
C | HBr | 浓硫酸与溴化钠 | 浓硫酸 | 水 |
D | CO | 甲酸与浓硫酸 | 浓硫酸 | 酸性KMnO4溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,⑦(NH4)2SO4,⑧乙醇中,由极性键形成的非极性分子有_______(填序号,以下同),含有金属离子的物质是__,分子间可形成氢键的物质是________,属于离子晶体的是__,属于原子晶体的是__,①~⑤五种物质的熔点由高到低的顺序是__。
(2)A,B,C,D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3500 ℃
试推断它们的晶体类型:A.__;B.__;C.__;D.__。
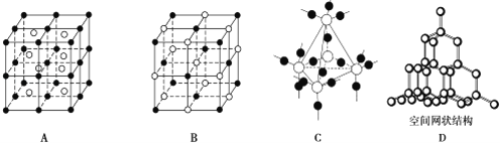
(3)下图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:A.__;B.__;C.__D.____。
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤气化和液化是现代能源工业中重点考虑的能源综合利用方案。最常见的气化方法为用煤生产水煤气,而当前比较流行的液化方法为用煤生产CH3OH。
(1)已知:CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH1
2CO(g)+O2(g)===2CO2(g) ΔH2
2H2(g)+O2(g)===2H2O(g) ΔH3
则反应CO(g)+2H2(g)===CH3OH(g)的ΔH=______。
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线。
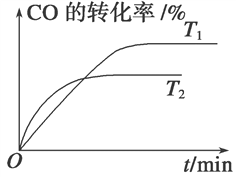
①T1和T2温度下的平衡常数大小关系是K1________K2(填“>”、“<”或“=”)。
②由CO合成甲醇时,CO在250 ℃、300 ℃、350 ℃下达到平衡时转化率与压强的关系曲线如下图所示,则曲线c所表示的温度为________ ℃。实际生产条件控制在250 ℃、1.3×104 kPa左右,选择此压强的理由是____________。

③以下有关该反应的说法正确的是________(填序号)。
A.恒温、恒容条件下,若容器内的压强不再发生变化,则可逆反应达到平衡
B.一定条件下,H2的消耗速率是CO的消耗速率的2倍时,可逆反应达到平衡
C.使用合适的催化剂能缩短达到平衡的时间并提高CH3OH的产率
D.某温度下,将2 mol CO和6 mol H2充入2 L密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为80%
(3)一定温度下,向2 L固定体积的密闭容器中加入1 mol CH3OH(g),发生反应:CH3OH(g) ![]() CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。
CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。
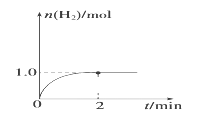
0~2 min内的平均反应速率v(CH3OH)=__________。该温度下,反应CO(g)+2H2(g) ![]() CH3OH(g)的平衡常数K=__________。相同温度下,在一个恒容容器中加入一定量的CO(g)和H2发生:CO(g)+2H2(g)
CH3OH(g)的平衡常数K=__________。相同温度下,在一个恒容容器中加入一定量的CO(g)和H2发生:CO(g)+2H2(g) ![]() CH3OH(g)的反应,某时刻测得体系中各物质的量浓度如下:C(CO)=0.25 mol·L-1,C(H2)=1.0 mol·L-1,C(CH3OH)=0.75 mol·L-1,则此时该反应_____进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
CH3OH(g)的反应,某时刻测得体系中各物质的量浓度如下:C(CO)=0.25 mol·L-1,C(H2)=1.0 mol·L-1,C(CH3OH)=0.75 mol·L-1,则此时该反应_____进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知强酸与强碱在稀溶液里反应的中和热可表示为:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1对下列反应:
CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH=-Q1kJ·mol-1
![]() H2SO4(浓)+NaOH(aq)=
H2SO4(浓)+NaOH(aq)=![]() Na2SO4(aq)+H2O(l) ΔH=-Q2kJ·mol-1
Na2SO4(aq)+H2O(l) ΔH=-Q2kJ·mol-1
HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-Q3kJ·mol-1
上述反应均在溶液中进行,则下列Q1、Q2、Q3的关系正确的是( )
A.Q2>Q3>Q1B.Q2>Q1>Q3C.Q1=Q2=Q3D.Q2=Q3>Q1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com