
| A. | 30mL 1.0mol/L NaCl溶液 | B. | 10mL2.0mol/L FeCl3溶液 | ||
| C. | 50mL1.5mol/L MgCl2溶液 | D. | 100mL1.0mol/L HCl溶液 |
分析 1.0mol/L AlCl3溶液中Cl-物质的量浓度为1.0mol/L×3=3mol/L,结合选项中溶质的浓度及构成计算离子的浓度,以此来解答.
解答 解:A.1.0mol/L NaCl溶液中Cl-物质的量浓度为1.0mol/L,故A不选;
B.2.0mol/L FeCl3溶液中Cl-物质的量浓度为2.0mol/L×3=6mol/L,故B不选;
C.1.5mol/L MgCl2溶液中Cl-物质的量浓度为1.5mol/L×2=3mol/L,故C选;
D.1.0mol/L HCl溶液中Cl-物质的量浓度为1.0mol/L,故D不选;
故选C.
点评 本题考查物质的量浓度的计算,为高频考点,把握溶质浓度与离子浓度的关系为解答该题的关键,侧重分析与计算能力的考查,注意物质的构成及电离,题目难度不大.


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 用小刀将金属钠切成小块 | |
| B. | 灼热的铁丝在Cl2中燃烧 | |
| C. | 刚切开的金属钠放置在空气中会变暗 | |
| D. | Cl2使湿润的红色纸条褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1)△H=-20Q kJ/mol | |
| B. | C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(l)△H=-40Q kJ/mol | |
| C. | $\frac{1}{2}$C2H5OH(1)+$\frac{3}{2}$O2(g)=CO2(g)+$\frac{3}{2}$H2O(g)△H=-20Q kJ/mol | |
| D. | C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(g)△H=-40Q kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14.7g | B. | 16.1g | C. | 15.5g | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 :3-甲基-3-戊醇
:3-甲基-3-戊醇 :4-甲基-2-戊烯
:4-甲基-2-戊烯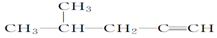 :4-甲基-1-戊炔
:4-甲基-1-戊炔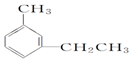 :1-甲基-3-乙苯(或间甲乙苯).
:1-甲基-3-乙苯(或间甲乙苯).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与硫酸铜溶液反应会置换出红色的铜 | |
| B. | 常温下干燥氯气与铁不反应,可以用钢瓶储存液氯 | |
| C. | SO2具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色 | |
| D. | 普通玻璃的组成可用Na2O•CaO•6SiO2表示,是纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 3.0×10-20 | 1.0×10-38 | 1.7×10-7 | 1.3×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
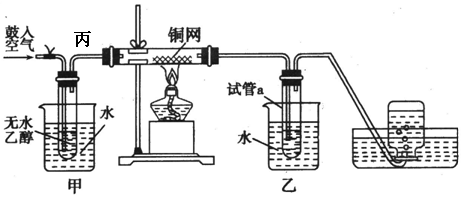
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com