
【题目】回答下列问题
(1)请写出一定条件下 Cu 与浓硫酸反应制取二氧化硫的化学方程式:___________。该反应中发生氧化反应的物质是__________,1mol氧化剂得到__________mol电子。
(2)PH< ______的雨称为酸雨。向煤中加入适量的______可大大减少燃烧产物中二氧化硫的含量。
(3)一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的浓度恰好相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比为__________。
【答案】Cu+2H2SO4(浓)![]() CuSO4 +SO2↑+2H2O Cu 2mol 5.6 石灰石或生石灰 2:3
CuSO4 +SO2↑+2H2O Cu 2mol 5.6 石灰石或生石灰 2:3
【解析】
(1)铜与浓硫酸加热反应生成硫酸铜、二氧化硫和水;该反应中Cu化合价升高,作为还原剂,发生氧化反应;H2SO4中S元素化合价由+6价下降到+4价,得到2个电子,1mol H2SO4反应得到2mol电子;
(2)pH< 5.6的雨称为酸雨,石灰石或生石灰可以和二氧化硫反应,故向煤中加入适量的石灰石或生石灰可大大减少燃烧产物中二氧化硫的含量;
(3)通过反应Fe+2Fe3+=3Fe2+中对应关系,计算已反应的Fe3+和未反应的Fe3+的物质的量之比。
(1)铜与浓硫酸加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式为:Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O;该反应中Cu化合价升高,作为还原剂,发生氧化反应;H2SO4中S元素化合价由+6价下降到+4价,得到2个电子,1mol H2SO4反应得到2mol电子;故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;该反应中Cu化合价升高,作为还原剂,发生氧化反应;H2SO4中S元素化合价由+6价下降到+4价,得到2个电子,1mol H2SO4反应得到2mol电子;故答案为:Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O;Cu;2mol;
CuSO4+SO2↑+2H2O;Cu;2mol;
(2) pH< 5.6的雨称为酸雨,石灰石或生石灰可以和二氧化硫反应,故向煤中加入适量的石灰石或生石灰可大大减少燃烧产物中二氧化硫的含量,故答案为:5.6;石灰石或生石灰;
(3)设已反应的Fe3+的物质的量为2mol,则:
Fe+2Fe3+=3Fe2+
2mol 3mol
溶液中Fe2+的物质的量为3mol,溶液中的Fe3+和Fe2+浓度相等,所以未反应的Fe3+的物质的量为3mol,则已反应的Fe3+和未反应的Fe3+的物质的量之比为2mol:3mol=2:3,故答案为:2:3。


科目:高中化学 来源: 题型:
【题目】降冰片烯(结构见 F)的衍生物在橡胶工业有重要用途。一种利用脱羰偶联反应合成其衍生物的路线如下:
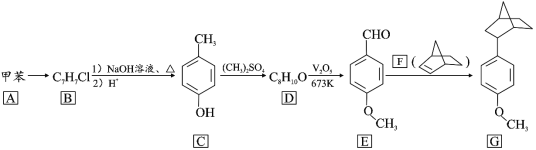
回答下列问题
(1)A→B 所需的试剂为_______________ 。
(2)B→C 第一步反应的化学方程式为_____。
(3)D 的结构简式为_____,C→D 的反应类型为_______。
(4)E 中的官能团名称为_____。
(5)芳香化合物X 是E 的同分异构体,X 能与热的NaOH 溶液反应生成稳定化合物, 0.1mol X 消耗 NaOH 0.2mol,化合物 X 共有_____种(不考虑立体异构)。其中核磁共振氢谱显示有 5 种不同化学环境的氢,峰面积比为 2∶2∶2∶1∶1 的结构简式为_____。
(6)参照上述路线,设计由苯甲醛、甲醇和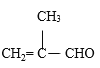 制备成
制备成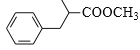 路线_____。(无机试剂任选)
路线_____。(无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型高性能电池的开发与研究已成为当下信息产业化时代的迫切要求、某研究团队设计研制了种高性能的磷酸铁锂(LiFePO4,简称LFP)电池。正极材料为磷酸铁锂,与Al相连,负极材料为石墨,与Cu相连,正、负之间存在电解质并通过聚合物隔膜隔开,此膜只允许Li+通过,其工作原理如图所示,总反应为Li(1-x)C6十LiFePO4![]() LiC6+ Li(1-x) FePO4。下列有关说法正确的是
LiC6+ Li(1-x) FePO4。下列有关说法正确的是
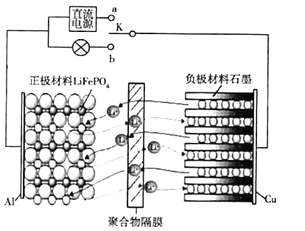
A.当开关K置于a时,Li+由右向左穿过聚合物隔膜到达正极
B.当开关K置于a时,正极材料上的电极反应为: Li(1-x) FePO4 +xLi ++xe- =LiFePO4
C.该电池的正、负极之间可以用Na2SO4水溶液作电解质溶液
D.当开关K置于b时,负极上的电极反应为:LiC6- xe- = Li(1-x) C6+xLi+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaHC2O4溶液的pH < 7。常温下,向pH=8.4的Na2C2O4溶液中滴加0.1mol/L的HCl溶液,溶液pH与pOH[pOH=-lgc(OH-)]的变化关系如图所示,下列各点所示溶液中微粒的物质的量浓度关系一定正确的是

A. a点:c(H+)+c(HC2O4-)+2c(H2C2O4)=c(OH-)
B. b点:c(Cl-)>c(H2C2O4)+c(HC2O4-)+c(C2O42-)
C. c点:c(Na+)=c(HC2O4-)+ c(C2O42-)+c(Cl-)
D. d点:c(OH-)+ c(Cl-)>c(H+)+2c(H2C2O4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质相互混合反应后,最终有白色沉淀生成的是( )
①过量Na2O2投入到CuCl2溶液中
②过量Ba(OH)2溶液和硫酸铝溶液混合
③少量Ca(OH)2投入过量NaHCO3中
④澄清石灰水中通入少量CO2
⑤CaCl2与NaOH的混合溶液中通入过量CO2
A.全部B.①⑤C.②③④D.②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)葡萄酒中SO2最大使用量为0.25 g·L-1,取300.00 mL葡萄酒,通过适当的方法使 所含SO2全部逸出并用H2O2将其全部氧化为H2SO4,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定。
①滴定前排气泡时,应选择下图中的________(填序号)。
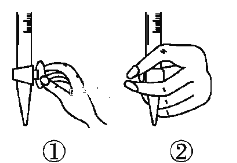
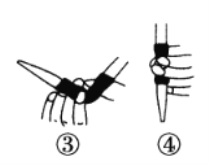
②若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积___(填序号)。
①=10 mL ②=40 mL ③<10 mL ④>40 mL。
③上述滴定实验中,可选择___为指示剂,选择该指示剂时如何判断反应到达滴定终点:_____。
④滴定终点读数时俯视刻度线,则测量结果比实际值________(填“偏高”、“偏低”或“无影响”)。
(2)某学生用0.100molL-1的KOH标准溶液滴定未知浓度的盐酸,其操作为:
A.移取20mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴处充满溶液;
D.取标准KOH溶液注入碱式滴定管至刻度“0”以上2~3cm 处;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管下面,用标准KOH溶液滴定至终点并记下刻度。
实验编号 | KOH溶液的浓度(mol/L) | 滴定完成时,KOH溶液滴入的体积(mL) | 待测盐酸溶液的体积(mL) |
1 | 0.10 | 22.62 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
①正确操作步骤的顺序是(用序号字母填写)___________________________
②根据上述数据,可计算出该盐酸的浓度约为______________(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】福酚美克是一种影响机体免疫力功能的药物,可通过以下方法合成:
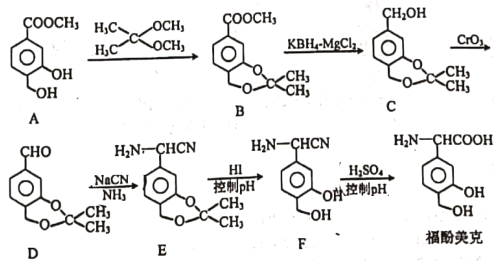
(1)B中的含氧官能团有________和_________(填名称);
(2)C→D的转化属于_________反应(填反应类型).
(3)已知E→F的转化属于取代反应,则反应中另—产物的结构简式为______。
(4) A (C9H10O4)的一种同分异构体X满足下列条件:
I.X分子有中4种不同化学环境的氢。
II. X能与FeCl3溶液发生显色反应。
III. lmol X最多能与4 mol NaOH发生反应
写出该同分异构体的结构简式:_____________。
(5)已知:![]()
![]()
![]() +R3CHO,根据已有知识并结合相关信息.
+R3CHO,根据已有知识并结合相关信息.
写出以  为原料制备
为原料制备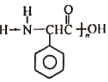 的合成路线流程图(无机试剂任用)。____________
的合成路线流程图(无机试剂任用)。____________
合成路线流程图示例如下:CH3CH2Br![]() CH3CH2OH
CH3CH2OH ![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定的条件下,下列选项所示的物质间转化均能实现的是( )
A.Na ![]() Na2O
Na2O![]() NaOH
NaOH
B.MgCO3![]() MgCl2
MgCl2![]() Mg
Mg
C.Al2O3![]() Al
Al![]() Fe
Fe
D.Fe2O3![]() FeCl3
FeCl3![]() FeCl2(aq)
FeCl2(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
(1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是______________(填序号)。
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2)写出制备Fe(OH)3胶体的化学反应方程式:________________。
(3)如何用最简单的方法判断(1)中是否成功制备胶体?_________________________。
(4)取少量制得的胶体加入试管中,再加入少量(NH4)2SO4溶液,观察到的现象是__________,这种现象称为胶体的________________。
(5)Fe(OH)3胶体能稳定存在的主要原因是________(填序号)。
A. 胶粒直径小于1nm B. 胶粒带正电荷
C. 胶粒作布朗运动 D . 胶粒能透过滤纸
(6)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是________(填序号)。
A.Fe(OH)3胶体粒子的直径在1~100nm之间 B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系 D.Fe(OH)3胶体的分散质粒子能透过滤纸
(7)向Fe(OH)3胶体中插入电极通电后,Fe(OH)3胶体粒子应该移向_______极,说明该胶体粒子带_____电;提纯Fe(OH)3胶体中混有的少量离子可以用的方法是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com