
分析 (1)原子基态时最外层具有6个p电子,s能级容纳2个电子,则最外层电子数为8;
(2)基态原子的3d亚层为半充满的所有元素即3d轨道上有5个电子,基态原子外围电子排布为3d54s2,3d54s1;
(3)基态原子的次外层d轨道全满,最外层有一个s电子,则基态原子外围电子排布为3d104s1;
(4)某元素+3价离子基态时和氩原子的电子构型相同,该元素质子数=18+3=21;
(5)原子半径第二小的主族元素为第二周期第ⅤⅡA族.
解答 解:(1)原子基态时最外层具有6个p电子,s能级容纳2个电子,则最外层电子数为8,处于零族,1~36号元素中有Ne、Ar、Kr;
故答案为:Ne、Ar、Kr;
(2)基态原子的3d亚层为半充满的所有元素即3d轨道上有5个电子,基态原子外围电子排布为3d54s2和3d54s1,为Mn、Cr元素,故答案为:Mn、Cr;
(3)基态原子的次外层d轨道全满,最外层有一个s电子,则基态原子外围电子排布为3d104s1,为Cu元素,故答案为:Cu;
(4)某元素+3价离子基态时和氩原子的电子构型相同,该元素质子数=18+3=21,为Sc元素,故答案为:Sc;
(5)原子半径第二小的主族元素为第二周期第ⅤⅡA族,为F元素,故答案为:F.
点评 本题考查核外电子排布以及结构与性质、位置关系,难度不大,注意对核外电子排布规律的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | 绿色植物的光合作用是把热能转化为化学能的过程 | |
| B. | 生物能是与化学反应无关的一种能源 | |
| C. | 化学能只能以热能的形式释放 | |
| D. | 葡萄糖在人体内的氧化是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锂离子电池和普通锌锰干电池都是二次电池 | |
| B. | 原电池的反应的本质是氧化还原反应 | |
| C. | 燃料电池是一种高效但是会污染环境的新型电池 | |
| D. | 铅蓄电池放电的时候正极是Pb负极是PbO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2使品红、酸性高锰酸钾溶液褪色,均体现SO2的漂白性 | |
| B. | 完全由非金属元素组成的化合物不一定是共价化合物 | |
| C. | 元素周期表有18列,就有18个族 | |
| D. | SO2的水溶液能导电,所以SO2是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶剂的质量 | B. | 溶质的质量分数 | C. | KNO3的溶解度 | D. | 溶液中K+的数目 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤ | B. | ①③④ | C. | ③④ | D. | ①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
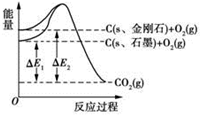 2013年7月23日人民网报道,河南省柘城县科技创新“创”出金刚石产业新天地.1mol石墨在一定条件下完全转化为金刚石,其能量变化如图所示,△E1=393.5kJ,△E2=395.4kJ,下列说法正确的是( )
2013年7月23日人民网报道,河南省柘城县科技创新“创”出金刚石产业新天地.1mol石墨在一定条件下完全转化为金刚石,其能量变化如图所示,△E1=393.5kJ,△E2=395.4kJ,下列说法正确的是( )| A. | 1 mol石墨完全转化为金刚石需吸收1.9 kJ的能量 | |
| B. | 石墨转化为金刚石属于物理变化 | |
| C. | 金刚石的稳定性强于石墨的 | |
| D. | 1 mol金刚石的能量大于1mol CO2的能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com