
下列物质的性质中,与氢键无关的是( )
A、甲醇极易溶于水 B、乙酸的熔点比甲酸甲酯高
C、氨气易液化 D、氟化氢非常稳定
【知识点】氢键的存在对物质性质的影响
【答案解析】D 解析:F、O、N的电负性较强,对应的氢化物分子之间能形成氢键,由于氢键的作用力大于范德华力,则含有氢键的物质熔沸点较高,易溶于水.
A、甲醇中的羟基能与水形成氢键,使甲醇在水中的溶解度增大,故与氢键有关;B、乙酸分子间能形成氢键,分子间氢键的存在导致使物质的熔沸点升高,所以乙酸比甲酸甲酯的熔点高C、氨气内部存在氢键,使得其溶沸点升高,所以氨气容易液化;D、氟化氢非常稳定是因为F元素的非金属性非常强,与氢键无关;
故答案选D
【思路点拨】本题考查氢键知识,侧重于氢键对物质的性质的影响,题目难度不大,学习中注意总结该部分知识.


科目:高中化学 来源: 题型:
下列有关问题,与盐的水解有关的是( )
①NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂 ②用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂 ③草木灰或铵态氮肥不能混合施用 ④实验室盛放Na2CO3溶液的试剂瓶不能用磨口玻璃塞 ⑤加热蒸干AlCl3溶液得到Al(OH)3固体
A.①②③ B.②③④ C.①④⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
A是芳香烃的含氧衍生物。为了测定其分子组成,进行如下实验:
①在一定温度和压强下将A气化,其气体的质量是同温、同压下等体积氦气质量的38倍;②称取7.6gA,在11.2L氧气中完全燃烧,其产物只有CO2和水蒸气。将反应后的混合气 通过浓硫酸后体积为10.64L,浓H2SO4质量增加3.6g。再将余下的气体通过盛有足量Na2O2的干燥管后,气体体积减少至6.16L(气体体积均在标准状况下测定)。试回答:
(1)A的分子式为 ;
(2)A物质苯环上只有一取代基,遇FeCl3溶液无显色反应。1molA只能与1molNaHCO3反应;1molA与足量Na反应生成1molH2。则A的结构简式为 ;
(3)A与足量钠反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
液晶高分子材料应用广泛,新型液晶基元﹣﹣化合物IV的合成线路如下:
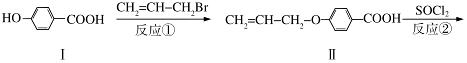

(1)化合物Ⅰ的分子式为 ,1mol化合物Ⅰ最多可与 mol NaOH反应。
(2)CH2=CH﹣CH2Br与NaOH水溶液反应的化学方程式为 (注明条件)。
(3)化合物I的同分异构体中,苯环上一溴代物只有2种且能发生银镜反应的化合物有多种,写出其中一种同分异构体的结构简式 (任写一种)。
(4)反应③的反应类型是 .在一定条件下,化合物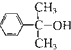 也可与III发生类似反应③的反应生成有机物V,V的结构简式是 。
也可与III发生类似反应③的反应生成有机物V,V的结构简式是 。
(5)下列关于化合物Ⅳ的说法正确的是 (填字母)。
A.属于烯烃 B.能与FeCl3溶液反应显紫色
C.一定条件下能发生加聚反应 D.能使溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
x 、y为两种元素的原子,x的阴离子与y的阳离子具有相同的电子层结构,由此可知 ( )
A. x的原子半径大于y的原子半径。 B. x的电负性小于y的电负性。
C. x 的氧化性小于y的氧化性。 D. x的第一电离能大于y 的第一电离能。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
(1)X元素基态原子核外电子排布式为________,该元素的名称是________。
(2)Y元素原子价电子排布图为 。
(3)X与Z可形成化合物XZ3,该化合物的空间构型为________。
(4)已知由元素X与镓元素组成的化合物A为第三代半导体。已知化合物A的晶胞结构与金刚石相似,其中X原子位于立方体内,镓原子位于立方体顶点和面心,请写出化合物A的化学式 ;化合物A可由(CH3)3Ga和XZ3在700℃下反应制得,反应的化学方程式为 。
(5)已知铝与镓元素位于同一主族,金属铝属立方晶系,其晶胞边长为405 pm,密度是2.70g·cm-3,通过计算确定其晶胞的类型 (填简单、体心或面心立方);晶胞中距离最近的铝原子可看作是接触的,计算铝的原子半径r(A1)= pm。(列出算式即可,已知:4053≈6.64×107)
查看答案和解析>>
科目:高中化学 来源: 题型:
五种短周期元素的某些性质如表所示(其中Z、M、W为同周期元素)。
| 元素代号 | Y | X | W | M | Z |
| 原子半径(×10-12 m) | 64 | 73 | 78 | 96 | 113 |
| 主要化合价 | -1 | +5、-3 | +7、-1 | +4、-4 | +3 |
下列说法不正确的是( )
A.由M与W形成的化合物是含有极性键的极性分子
B. X与M之间形成的化合物,其晶体是原子晶体
C.由M元素形成的晶体,是太阳能光伏发电的主要材料,工业上制取M单质,可通过置换反应原理来生产
D.Y与Z元素形成的[ZY6]3-,离子中存在配位键,该离子构型呈正八面体
查看答案和解析>>
科目:高中化学 来源: 题型:
普罗帕酮为广谱高效膜抑制性抗心律失常药。其合成路线如下:
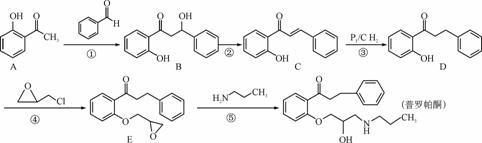
(1) 化合物C的含氧官能团为________和________(填官能团的名称)。
(2) 反应①→④中属于加成反应的是________(填序号)。
(3) 写出同时满足下列条件的A的同分异构体结构简式:________。
Ⅰ. 分子中含有苯环,且苯环上的一氯代物有两种;
Ⅱ. 与FeCl3溶液发生显色反应;
Ⅲ. 能发生银镜反应。
(4) 产物普罗帕酮中会混有少量副产物F(分子式为C21H27O3N)。F的结构简式为________。
(5) 化合物3羟基戊二酸二乙酯(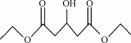 )是一种医药中间体,请结合流程信息,写出以丙酮、乙醇和甲醛为原料,制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
)是一种医药中间体,请结合流程信息,写出以丙酮、乙醇和甲醛为原料,制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
H2C==CH2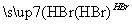 CH3CH2Br
CH3CH2Br CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是
A.向碳酸氢钠溶液中滴入氢氧化钠 HCO3-+OH-=CO32-+H2O
B.向碳酸氢钾溶液中滴入过量澄清石灰水 2HCO3-+Ca2++2OH-=CO32-+2H2O+CaCO3↓
C.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:
Ba2++OH-+H++SO42- ==BaSO4↓+H2O
D.硫酸铜和氢氧化钡溶液混合SO42-+Ba2+=+BaSO4↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com