
下列变化中,吸收的热量用于克服分子间作用力的是
A.加热金属铝使之熔化 B.加热金刚石使之熔化
C.液溴受热变成溴蒸气 D.加热碘化氢使之分解
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
[化学——选修2:化学与技术](14分)
纯碱(化学式为Na2CO3)是一种重要的化工原料。现代化工生产有三种工艺:
(一)布兰制碱法。以食盐为原料制碱,该法分三步:
①用氯化钠与硫酸反应制硫酸钠:2NaCl+H2SO4=Na2SO4+2HCl;
②用焦炭还原硫酸钠得硫化钠:Na2SO4+4C=Na2S+4CO↑
③用硫化钠与石灰石反应制碳酸钠:Na2S+CaCO3=Na2CO3+CaS
(二)氨碱法即索尔维制碱法。以食盐、氨、二氧化碳为原料,其反应也分三步进行:
①NH3+CO2+H2O=NH4HCO3
②NH4HCO3+NaCl=NaHCO3+NH4Cl
③2NaHCO3=Na2CO3+CO2↑+H2O
(三)候氏制碱法。低温下先向饱和食盐水中通入氨气,再通入二氧化碳可析出碳酸氢钠,再加入细盐末,因同离子效应,低温氯化铵溶解度突然降低,而食盐的溶解度变化不大,所以氯化铵析出而食盐不析出;再用氨饱和后通二氧化碳,结果往返析出NaHCO3和NH4Cl。该法生产的纯碱质量优良,纯白如雪。
(1)相比另外两种方法,布兰制碱法工艺的缺点除了成本较高,生成CO和CaS等污染物外还有__________________________和_____________________________(写两点)。
(2)氨碱法工艺的中循环利用的物质是_________(填化学式);产品的副产物NH4Cl既可以做氮肥又可以重新生成氨气。写出NH4Cl与生石灰反应的化学方程式 。
(3)候氏制碱法反应的方程式为____________________________________________。
(4)为什么候氏制碱法工艺中先向饱和食盐水中通入氨气,再通入二氧化碳。理由是__________________________________________________(写一点)。
(5)候氏制碱法产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,用m1表示加热前纯碱样品的质量,m2表示加热后固体的质量。则纯碱中碳酸氢钠的质量分数可表示为:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
绿色交通工具是指在行驶中对环境不发生污染或只发生微量污染的载客工具。下列不属于绿色交通工具的是

A.无轨电车 B.氢气动力车 C.太阳能汽车 D.柴油汽车
查看答案和解析>>
科目:高中化学 来源: 题型:
下列图示与对应的叙述正确的是
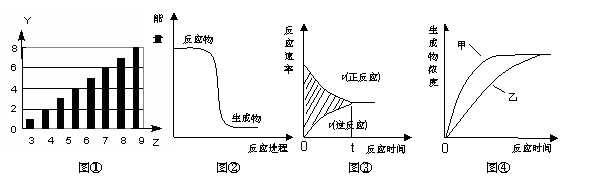
A.图①所示柱形图,纵坐标表示第二周期元素最高正价随原子序数的变化
B.图②所示曲线,表示该反应是吸热反应
C.图③所示曲线的阴影部分面积,表示正反应速率改变值
D.图④所示曲线,甲、乙分别表示有、无催化剂时发生的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
前苏联科学家欧巴林教授在其著作中曾说:“生命起源于甲烷”,英国科学家巴纳尔教授则认为生命是从二氧化碳及水开始的。与之相关的转化关系如下图所示(部分反应条件已略去)。
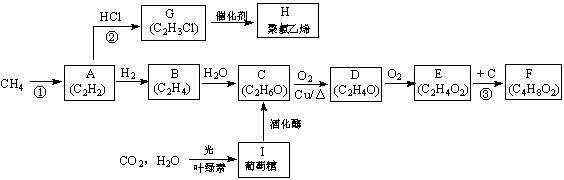 (1)C中官能团的电子式为 ▲ ;反应②的类型为 ▲ 。
(1)C中官能团的电子式为 ▲ ;反应②的类型为 ▲ 。
(2)写出结构简式:D为 ▲ ;H为 ▲ 。
(3)反应③的化学方程式为 ▲ ;二氧化碳及水光合作用生成葡萄糖的化学方程式为
▲ 。
(4)在自然界纤维素与水可在甲烷菌催化下水解生成甲烷和二氧化碳,写出该反应的化学方程式并配平: ▲ 。
(5)已知:断开1mol共价键吸收的能量或形成1mol共价键释放的能量数据如下表
| 共价键 | H—H | C—H | C≡C |
| 能量变化/kJ·mol-1 | 436 | 413 | 812 |
反应① 2CH4(g) →C2H2(g) +3H2(g) △H= ▲ kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
巴豆酸的结构简式为CH3—CH=CH—COOH。现有:①氯化氢 ②溴水 ③纯碱溶液④乙醇 ⑤酸性高锰酸钾溶液,试根据巴豆酸的结构特点,判断在一定条件下,能与巴豆酸反应的物质是
A.只有②④⑤ B.只有①③④ C.只有①②③⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
|
 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | ||||
| 二 | ① | ② | ③ | ④ | ||||||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)非金属性最强的元素是______(填元素符号,下同),形成化合物种类最多的元素是________。
(2)第三周期元素除⑩外原子半径最小的是______(填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是__________(填化学式,下同),具有两性的是____________。
(3)⑤⑥⑦单质的活泼性顺序为______>______>______ (填元素符号),判断的实验依据是________________________________________________ (写出一种)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com