
下列实验事实或实验现象,反映了硫酸的哪些性质?
(1)浓硫酸露置在空气中质量增加.___________________________
(2)浓硫酸和食盐反应可生成NaHSO4和Na2SO4两种盐.________
(3)浓硫酸和NaNO3反应可制备硝酸.________________________
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
| 实验步骤 | 实验现象 |
| 将打磨过的铝片(过量)放入一定浓度的CuCl2溶液中 | 产生气泡,析出疏松的红色固体,溶液逐渐变为无色 |
反应结束后分离出溶液备用 |
|
| 红色固体用蒸馏水洗涤后,置于潮湿空气中 | 一段时间后固体由红色变为绿色[其主要成分为Cu2(OH)2CO3] |
查看答案和解析>>
科目:高中化学 来源: 题型:
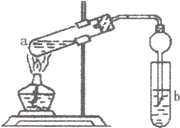 (1)下列实验操作或对实验事实的叙述正确的是
(1)下列实验操作或对实验事实的叙述正确的是查看答案和解析>>
科目:高中化学 来源:2011-2012学年安徽省六安三中高一下学期期末考试化学B卷(带解析) 题型:实验题
(12分)(1)下列实验操作或对实验事实的叙述正确的是__(填序号)
| A.用托盘天平称取4.00g干燥的NaOH固体,溶解于6ml蒸馏水中,配制10%NaOH溶液;配制氢氧化铜悬浊液,在一定量硫酸铜溶液中,加入少量10%氢氧化钠溶液。 |
| B.实验室蒸馏石油时,在蒸馏烧瓶中加入一些碎瓷片,防止暴沸;冷凝管下口进冷水,上口出热水。 |
| C.钠是活泼金属,易和空气中氧气、水反应,实验室将钠保存在无水酒精中。 |
| D.煤是由无机物和有机物组成的复杂混合物,其中含有苯、甲苯、二甲苯等有机物,可以用干馏方法获得苯。 |

查看答案和解析>>
科目:高中化学 来源:2014届安徽省高一下学期期末考试化学B卷(解析版) 题型:实验题
(12分)(1)下列实验操作或对实验事实的叙述正确的是__(填序号)
A.用托盘天平称取4.00g干燥的NaOH固体,溶解于6ml蒸馏水中,配制10%NaOH溶液;配制氢氧化铜悬浊液,在一定量硫酸铜溶液中,加入少量10%氢氧化钠溶液。
B.实验室蒸馏石油时,在蒸馏烧瓶中加入一些碎瓷片,防止暴沸;冷凝管下口进冷水, 上口出热水。
C.钠是活泼金属,易和空气中氧气、水反应,实验室将钠保存在无水酒精中。
D.煤是由无机物和有机物组成的复杂混合物,其中含有苯、甲苯、二甲苯等有机物,可以用干馏方法获得苯。
E.多数有机反应很慢,往往需要加热,采用水浴加热易控制温度且受热均匀,石油分馏、苯和浓硝酸发生取代反应、银镜反应、油脂水解均必需水浴加热。
F.用渗析法分离淀粉中混有的NaN03杂质,用盐析方法提纯蛋白质。
(2)如右图,在试管a中先加入2mL95%的乙醇,边摇动边缓缓加入5mL浓H2S04并充分摇匀,冷却后再加入2g无水醋酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入 7mL饱和碳酸钠溶液。连接好装置。用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验。
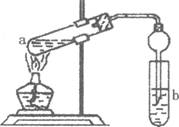
①加人浓H2S04的作用是______________________________________
②试管b中观察到的主要现象是_________________________________
③在实验中球形干燥管除起冷凝作用外,另一个重要作用是___________________________
④饱和Na2C03溶液的作用是__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
①向试管中滴加液体时,为不使液体滴到试管外应将胶头滴管伸入试管中;
②配置100 mL 1.00mol/L的NaCl溶液时,可用托盘天平称取5.85 gNaCl固体;
③向100℃时的NaOH稀溶液中滴加饱和的FeCl3溶液,以制备Fe(OH)3胶体;
④配制氯化铁溶液时,先将氯化铁固体加入盐酸中溶解,然后加水稀释;
⑤分液漏斗分液时,先将下层的液体从下口流出,然后再从下口流出上层的液体
⑥测定某溶液pH时,取一小块干燥的试纸放入玻璃片上,用玻璃棒蘸取溶液滴
在试纸的中部,再与pH试纸比色卡对比(2)在下图所示的实验装置中,盛有足量水的水槽里放两个烧杯,小烧杯里放有少量铜片和过量浓硝酸,小烧杯外面倒扣一大烧杯,清回答下列问题:
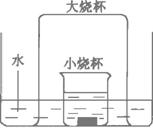
Ⅰ.实验过程中,观察到的主要现象是:
①铜片表面产生气泡,铜片变小并逐渐消失;
②小烧杯中溶液的颜色逐渐变成绿色;
③________________________________________________。
④________________________________________________。
Ⅱ.用该装置做铜与浓硝酸反应的实验,最突出的优点是______________。
Ⅲ.若要验证最终得到的气体生成物,最简便的方法是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com