
| A.0.5 mol O3与11.2 L O2所含的分子数一定相等 |
| B.常温常压下,78 g Na2O2和Na2S的混合物中含有的阴离子数为NA |
C.2SO2(g)+O2(g) 2SO3(g)和SO2(g)+ 2SO3(g)和SO2(g)+ O2(g) O2(g) SO3(g)的ΔH相等 SO3(g)的ΔH相等 |
| D.物质的量浓度为0.25 mol/L的MgCl2溶液中,含有Cl-个数为0.5NA |
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 Al2(SO4)3+
Al2(SO4)3+ S
S
 Al2O3+
Al2O3+ ______↑。
______↑。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
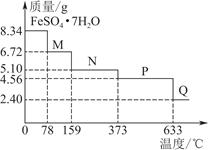
| A.FeSO4·7H2O晶体中有4种不同结合力的水分子 |
| B.在100 ℃时,M的化学式为FeSO4·6H2O |
| C.在200 ℃时,N的化学式为FeSO4·3H2O |
D.380 ℃的P加热至650 ℃的化学方程式为2FeSO4 Fe2O3+SO2↑+SO3↑ Fe2O3+SO2↑+SO3↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 NA,则下列各量不相等的是( )
NA,则下列各量不相等的是( )| A.消耗H2O和D2O的物质的量 |
| B.同温同压下生成气体的体积 |
| C.反应后所得溶液中溶质的质量分数 |
| D.参加反应的钾的质量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.62 g Na2O溶于水后所得溶液中含有的O2-数为NA |
| B.在含Al3+总数为NA的AlCl3溶液中,Cl-总数大于3NA |
| C.常温常压下,16 g甲基(—13CH3)所含的中子数为10NA |
| D.0.5 mol Cu和足量浓硝酸反应可以生成22.4 L NO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.标准状况下,22.4 L乙烯含有的共用电子对数为2 |
B.常温下,含有1 mol NaHSO4溶液中的阳离子数为 |
C.通常状况下,1 mol NO和0.5 molO2在密闭容器中混合,生成NO2分子数为 |
D.制取漂白粉时,标准状况下22.4 LCl2参加反应,转移电子数为 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.25 ℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| B.常温下,1 L 0.1 mol·L-1的NH4NO3溶液中氮原子数为0.2NA |
| C.10 L pH=1的硫酸溶液中含有的H+为2NA |
| D.欲配制1.00 L 1.00 mol·L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com