
【题目】化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
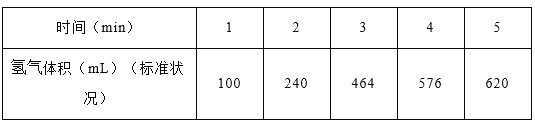
①哪一时间段反应速率最大______min(填0~1、1~2、2~3、3~4、4~5),原因是_____。
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率_________(设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是____。
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
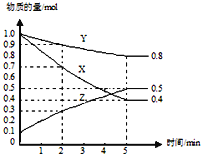
①该反应的化学方程式是_______。
②该反应达到平衡状态的标志是______
A.Y的体积分数在混合气体中保持不变
B.X、Y的反应速率比为3∶1
C.容器内气体压强保持不变
D.容器内气体的总质量保持不变
E.生成1mol Y的同时消耗2mol Z
③2min内Y的转化率为______。
【答案】 2~3 因该反应是放热反应,此时温度高且盐酸浓度较大,所以反应速率较快 0.025 mol/(Lmin) CD 3X(g)+Y(g)![]() 2Z(g) AC 10%
2Z(g) AC 10%
【解析】(1)①在0~1、1~2、2~3、3~4、4~5min时间段中,产生气体的体积分别为100mL、140mL、224mL、112mL、54mL,由此可知反应速率最大的时间段为2~3 min;原因是:因该反应是放热反应,此时温度高且盐酸浓度较大,所以反应速率较快;②在3~4min时间段内,n(H2)=0.112L/22.4L·mol-1=0.005mol,根据2HCl~H2,计算消耗盐酸的物质的量为0.01mol,则υ(HCl)=0.01mol/(0.4L·1min)=0.025mol/(L·min);③A.加入蒸馏水,H+浓度减小,反应速率减小且不减少产生氢气的量,故A正确;B.加入KCl溶液,H+浓度减小,反应速率减小且不减少产生氢气的量,故B正确;C.加入KNO3溶液,H+浓度减小,因酸性溶液中有NO3-,具有强氧化性,与Zn反应无氢气生成,故C错误;D.加入CuSO4溶液,Zn置换出Cu,形成原电池,反应速度增大,且影响生成氢气的量,故D错误;故选CD;(3)①由图象可以看出,反应中X、Y的物质的量减少,应为反应物,Z的物质的量增多,应为生成物,当反应进行到5min时,△n(Y)=0.2mol,△n(Z)=0.4mol,△n(X)=0.6mol,则△n(Y):△n(Z):△n(X)=1:2:3,参加反应的物质的物质的量之比等于化学计量数之比,则反应的方程式为:3X(g)+Y(g)![]() 2Z(g);②A.体积固定,混合气体的总物质的量不确定,Y的体积分数在混合气体中保持不变,反应达到平衡状态,故A正确;B.X、Y的反应速率比为3∶1,随着反应的进行X、Y的反应速率比始终为3:1,不能作为平衡状态的标志,故B错误;C.体积固定,混合气体的总物质的量不确定,当容器的压强保持一定,说明正逆反应速率相等,达平衡状态,故C正确;D.反应物生成物均为气体,容器内气体的总质量保持不变,不能作为平衡状态的标志,故D错误;E.生成1mol Y的同时消耗2mol Z 均只能表示逆速率,不能说明正逆反应速率相等,无法判断反应达到平衡状态,故E错误;故选AC。③2min内X的转化率为=变化物质的量/起始总物质的量 ×100%=(1mol-0.9mol)/1mol ×100%=10%.
2Z(g);②A.体积固定,混合气体的总物质的量不确定,Y的体积分数在混合气体中保持不变,反应达到平衡状态,故A正确;B.X、Y的反应速率比为3∶1,随着反应的进行X、Y的反应速率比始终为3:1,不能作为平衡状态的标志,故B错误;C.体积固定,混合气体的总物质的量不确定,当容器的压强保持一定,说明正逆反应速率相等,达平衡状态,故C正确;D.反应物生成物均为气体,容器内气体的总质量保持不变,不能作为平衡状态的标志,故D错误;E.生成1mol Y的同时消耗2mol Z 均只能表示逆速率,不能说明正逆反应速率相等,无法判断反应达到平衡状态,故E错误;故选AC。③2min内X的转化率为=变化物质的量/起始总物质的量 ×100%=(1mol-0.9mol)/1mol ×100%=10%.


科目:高中化学 来源: 题型:
【题目】某温度下,在2 L恒容密闭容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图所示,反应在t1 min 时达到平衡。
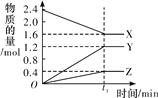
(1)请写出该反应的化学方程式:_____________________________。
(2)若上述反应中X、Y、Z分别为NH3、H2、N2,且已知1 mol 氨气分解成氮气和氢气要吸收46 kJ的热量,则至t1 min时,该反应吸收的热量为________;在此t1 min时间内,用H2表示该反应的平均速率v(H2)为__________。下列叙述能判断该反应达到平衡状态的是________(填字母代号)。
A.容器内各气体组分的质量分数不再发生改变
B.正反应速率与逆反应速率相等
C.容器内气体的密度不再发生改变
D.混合气体的平均相对分子质量不再发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。某厂为了变废为宝,将工业废水(含5.00×10-3 mol·L-1的Cr2O72-)处理得到磁性材料Cr0.5Fe1.5FeO4,设计了如下实验流程:
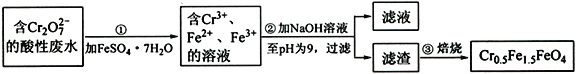
(1)第①步反应的离子方程式是________________________________。
(2)第②步过滤得到的滤渣中主要成分除Cr(OH)3外,还有____________________。
(3)为保证磁性材料的质量,应控制第①步反应后所得溶液中Fe2+与Fe3+的比例为______________。在第②步过程中,须持续通入N2,原因是________________________________。
(4)将FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeCO3的浊液。浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是________________________________。
(5)某研究性学习小组欲从蚀刻镀铜电路板所得废液(溶质为FeCl2、CuCl2、FeCl3)出发,制备FeCl3·6H2O,请设计制取FeCl3·6H2O的实验步骤:___________________________。 (可选用的试剂:铁粉、盐酸和H2O2溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.1molN2中含有的分子数为2×6.02×1023
B.用激光笔照射CuSO4溶液可产生“丁达尔效应”
C.常温下,铝片能溶于浓硫酸
D.常温下,淀粉溶液遇I2变为蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X,Y,Z,W,Q在元素周期表中的相对位置如图所示.下列说法正确的是( ) 
A.元素X与元素Z的最高正化合价之和的数值等于8
B.原子半径的大小顺序为:rX>rY>rZ>rW>rQ
C.离子Y2﹣和Z3+的核外电子数和电子层数都不相同
D.元素W的最高价氧化物对应的水化物的酸性比Q的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨为重要化工原料,有广泛用途。
(1)合成氨中的氢气可由下列反应制取:
a.CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H=+216.4kJ/mol
CO(g)+3H2(g) △H=+216.4kJ/mol
b.CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41.2kJ/mol
CO2(g)+H2(g) △H=-41.2kJ/mol
则反应CH4(g)+2H2O(g)![]() CO2(g)+4H2(g) △H=_________。
CO2(g)+4H2(g) △H=_________。
(2)起始时投入氮气和氢气分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度关系如下图。
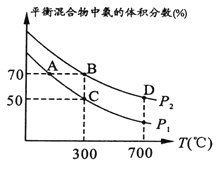
①恒压时,反应一定达到平衡状态的标志是______(填序号);
A.N2和H2的转化率相等 B.反应体系密度保持不变
C. ![]() 比值保持不变 D.
比值保持不变 D. ![]() =2
=2
②P1_____P2(填“>”、“<”、“=”、“不确定”,下同);反应平衡常数:B点____D点;
③C点H2的转化率____;在A、B两点条件下,该反应从开始到平衡时生成氨气平均速率:v(A)______v(B)。
(3)N2H4可作火箭推进剂,NH3和NaClO在一定条件下反应可生成N2H4。
①写出NH3和NaClO反应生成N2H4的化学方程式__________;
②已知25℃时N2H4水溶液呈弱碱性:N2H4+H2O![]() N2H5++OH- K1=1×10-a;N2H5++H2O
N2H5++OH- K1=1×10-a;N2H5++H2O![]() N2H62++OH- K2=1×10-b。
N2H62++OH- K2=1×10-b。
25℃时,向N2H4水溶液中加入H2SO4,欲使c(N2H5+)>c(N2H4),同时c(N2H5+)>c(N2H62+),应控制溶液pH范围_________(用含a、b式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中X是一种具有水果香味的合成香料,A是直链有机物,E与FeCl3溶液作用显紫色.请根据上述信息回答: 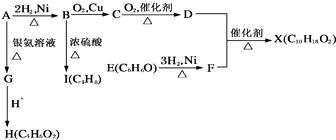
请回答下列问题:
(1)H中含氧官能团的名称是 . B→I的反应类型为 .
(2)只用一种试剂鉴别D、E、H,该试剂是 .
(3)D和F反应生成X的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体区别于其它分散系的本质是()
A. 胶体粒子不能穿过半透膜,能通过滤纸空隙
B. 胶体粒子带电荷并且在一定条件下能稳定存在
C. 胶体的分散质粒子直径在1 nm~100nm之间
D. 胶体粒子能够发生布朗运动而且能产生丁达尔现象
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com