
| A. | 1mol某气体的体积为22.4L,该气体的状况不一定是标准状况 | |
| B. | 1 mol H2O中含有的质子数为9NA | |
| C. | 2.4g镁由原子变为离子时,失电子为0.1NA | |
| D. | 将1mol CO2气体变成固体,其所含的分子数小于NA |
分析 A、根据pV=nRT可知,1mol气体的体积为22.4L,所处的条件有很多,不一定是标准状况;
B、1个水分子中含有10个电子;
C、依据n=$\frac{m}{M}$计算物质的量,结合镁原子最外层电子数为2计算;
D、1mol任何物质含有分子数为NA.
解答 解:A、1mol气体的体积为22.4L,根据pV=nRT可知,满足条件的T、P很多,不一定是标准状况,故A正确;
B、依据水分子含10个电子,1 mol H2O中含有的质子数为10NA,故B错误;
C、依据n=$\frac{m}{M}$计算物质的量=$\frac{2.4g}{24g/mol}$=0.1mol,结合镁原子最外层电子数为2计算镁由原子变为离子时,失电子为0.2NA,故C错误;
D、1mol任何物质含有分子数为NA,将1mol CO2气体变成固体,其所含的分子数等于NA,故D错误;
故选A.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积的条件分析判断,物质结构的理解应用,掌握基础是解题关键,题目较简单.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:解答题
 A、B、C、D分别是由两种短周期元素组成的常见微粒(或粒子),这四种微粒中均含有相同数目的电子,且共含有三种元素,其中A中含有5个原子核,它们之间有如下的反应关系.
A、B、C、D分别是由两种短周期元素组成的常见微粒(或粒子),这四种微粒中均含有相同数目的电子,且共含有三种元素,其中A中含有5个原子核,它们之间有如下的反应关系. 、D
、D .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
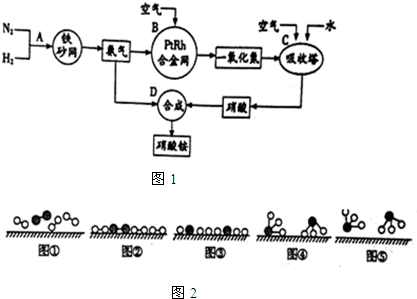
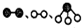 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面;在催化剂表面N2、H2中的化学键断裂.
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面;在催化剂表面N2、H2中的化学键断裂.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
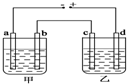 甲、乙两个相同的电解槽,如图所示连接a,b,c,d均为铂电极,通电后发现a极板处有气体放出,c极板质量增加,则以下说法中正确的是( )
甲、乙两个相同的电解槽,如图所示连接a,b,c,d均为铂电极,通电后发现a极板处有气体放出,c极板质量增加,则以下说法中正确的是( )| A. | 甲槽中溶液是H2SO4,乙槽中溶液是NaOH | |
| B. | 甲槽中溶液是NaOH,乙槽中溶液是AgNO3 | |
| C. | 甲槽中溶液是AgNO3,乙槽中溶液是CuSO4 | |
| D. | 甲槽中溶液是CuSO4,乙槽中溶液是H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②④ | C. | ②③ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
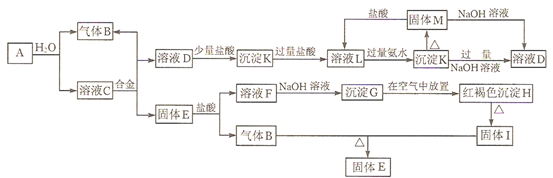
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲同学认为氯化铵由N、H、Cl三种元素组成 | |
| B. | 乙同学认为一个氯化铵分子中含有一个NH4+和一个Cl- | |
| C. | 丙同学认为氯化铵由NH4+和Cl-构成 | |
| D. | 丁同学认为氯化铵中阴、阳离子个数比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
 ,①、②、③原子半径从大到小的顺序是①②③
,①、②、③原子半径从大到小的顺序是①②③查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com