
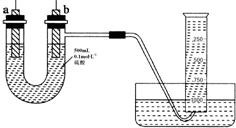
 现有纯锌片、纯铜片和500mL 0.1mol•L-1的硫酸、导线、1 000mL量筒.用如下图所示装置利用原电池原理,制备一定量的氢气.
现有纯锌片、纯铜片和500mL 0.1mol•L-1的硫酸、导线、1 000mL量筒.用如下图所示装置利用原电池原理,制备一定量的氢气.分析 锌、铜、硫酸原电池中,电子转移和产生的氢气量之间存在联系;
(1)根据原电池装置的构成条件:闭合回路、电解质溶液、两个电极以及自发氧化还原反应来回答;
(2)活泼失电子的金属锌做负极,发生氧化反应,电子由负极流向正极;
(3)铜作正极,发生还原反应,根据硫酸根离子流向负极判断a极附近SO42-浓度;
(4)根据电极反应式进行计算即可.
解答 解:(1)根据图示装置,要想求得电子转移的量,需要设计成锌、铜、硫酸原电池,量取金属锌和硫酸反应产生氢气的体积,根据原电池的构成条件,所以首先要用导线把a、b两电极连接起来,
故答案为:用导线把a、b两电极连接起来;
(2)锌、铜、硫酸原电池中,纯锌片是负极,电子由负极流向正极,故答案为:纯锌片;负;①;
(3)铜是正极,该极上电极反应为:2H++2e-=H2↑,硫酸根离子流向负极,所以a极附近SO42-浓度逐渐减小,
故答案为:2H++2e-=H2↑;逐渐减小;
(4)正极上电极反应为:2H++2e-=H2↑,当硫酸浓度降低一半时即消耗氢离子为0.5×0.1×$\frac{1}{2}$×2=0.05moL,所以通过导线的电子的物质的量为0.05mol,标况下生成$\frac{0.05}{2}$=0.025mol氢气,标况下的体积为0.025×22.4=560ml,量筒中收集的气体体积最接近600ml,
故答案为:0.05 mol; C.
点评 本题以实验方式为载体考查学生原电池的构成条件和工作原理知识,注意基本知识的梳理是解题关键,难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
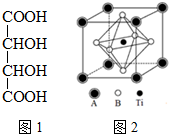 钛的化合物如TiSe2、Ti(NO3)4、TiCl4、酒石酸钛等均有着广泛用途.
钛的化合物如TiSe2、Ti(NO3)4、TiCl4、酒石酸钛等均有着广泛用途.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ①③⑥ | C. | ③④⑤ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子核外电子排布决定了该原子的化学性质 | |
| B. | 根据原子序数可以推知该原子的中子数和其在周期表中的位置 | |
| C. | ${\;}_{19}^{40}$K、${\;}_{20}^{40}$Ca是具有相同质量数的同位素原子 | |
| D. | 所有的原子核都是由质子和中子组成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HnX | B. | H(2m-n)X | C. | H(8+n-2m) X | D. | H(8+2m-n) X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢铁在弱碱性条件下发生电化学腐蚀的正极反应是:O2+2H2O+4e-═4OH- | |
| B. | 当镀锌铁制品的镀层破损时,镀层仍能对铁制品起保护作用 | |
| C. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 | |
| D. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述电解过程中共转移2 mol电子 | |
| B. | 原混合溶液中c(K+)为2 mol/L | |
| C. | 电解得到的Cu的物质的量为0.5 mol | |
| D. | 电解后溶液中c(H+)为2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 催化剂V2O5不改变该反应的逆反应速率 | |
| B. | 增大反应体系的压强,反应速率一定增大 | |
| C. | 一段时间内生成1 mol O2(g)同时生成1 mol SO3(g),说明反应达到平衡 | |
| D. | 在t1、t2时刻,SO3(g)的浓度分别是c1、c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为v=$\frac{{c}_{2}-{c}_{1}}{{t}_{2}-{t}_{1}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com