
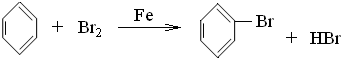 ,属于取代反应;
,属于取代反应;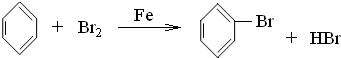 ;取代反应;
;取代反应; CH3COOC2H5+H2O,属于取代反应或者酯化反应;
CH3COOC2H5+H2O,属于取代反应或者酯化反应; CH3COOC2H5+H2O; 酯化反应(或取代反应).
CH3COOC2H5+H2O; 酯化反应(或取代反应).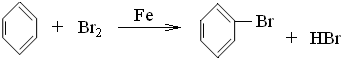 ;
; CH3COOC2H5+H2O.
CH3COOC2H5+H2O.

 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
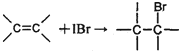
查看答案和解析>>
科目:高中化学 来源: 题型:
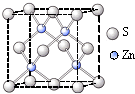
(12分)固体A是离子晶体,结构类似于CsCl,组成中含氮的质量分数为73.68%,它的所有原子的最外层都符合相应的稀有气体原子的最外层电子结构。该物质适当加热就分解成两种气体单质。试回答下列问题:
1.写出A的化学式 ,A的电子式 ;阳离子的结构为 体,其中心原子的杂化形态为 。
2.A溶于水后溶液呈 性(填“酸”、“碱”或“中”),其原因是(用化学方程式表示) 。
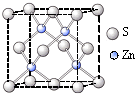
3.A与CuI在一定条件下可合成一种化合物B。B是一种红棕色、难溶于水的固体,X一射线衍射证实B是一种六方晶体,结构类同于闪锌矿(ZnS)测后的化学式为_________;生成B的化学反应为 。将B投入酸性溶液中(如盐酸溶液)可能看到的现象为 ,其化学反应方程式为 。
4.写出A受热分解的化学反应方程式 。该反应 (填“是”或“否”)属于氧化还原反应。
查看答案和解析>>
科目:高中化学 来源:2011年江苏省宿迁市泗阳县致远中学高考化学模拟试卷(解析版) 题型:解答题



查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com