
质量为8.02 g的铁片,放进1.0 L 0.90 mol·L-1 CuSO4溶液中,过一段时间取出洗净、干燥后称量,变为8.66 g,若认为溶液的体积没有变化,则反应后溶液中Cu2+的浓度为( )
A.0.89 mol·L-1 B.0.82 mol·L-1
C.0.78 mol·L-1 D.0.6 mol·L-1
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
A.0.89 mol·L-1 B.0.82 mol·L-1
C.0.78 mol·L-1 D.0.6 mol·L-1
查看答案和解析>>
科目:高中化学 来源:0119 期中题 题型:填空题
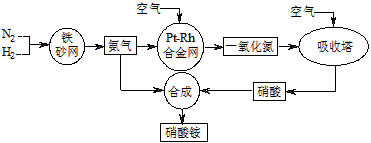
 2NH3(g) ΔH=-92 kJ·mol-1。
2NH3(g) ΔH=-92 kJ·mol-1。 查看答案和解析>>
科目:高中化学 来源: 题型:
A.
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com