
| A. | H2SO4 | B. | C2H5OH | C. | 稀HNO3 | D. | NaOH溶液 |
分析 铜丝灼烧变成黑色,则金属铜氧化生成了氧化铜,氧化铜可以和硫酸、乙醇、硝酸在一定的条件下反应,如反应前后质量不变,则CuO应被还原生成Cu,以此解答该题.
解答 解:A.铜丝灼烧成黑色,立即放入硫酸中,CuO与硫酸反应,生成铜盐,铜丝变红,铜丝质量减少,故A错误;
B.铜丝灼烧成黑色,立即放入C2H5OH中,CuO与C2H5OH反应:CuO+C2H5OH$\frac{\underline{\;\;△\;\;}}{\;}$CH3CHO+Cu+H2O,反应后铜丝变红,质量保持不变,故B正确;
C.铜丝灼烧成黑色,立即放入稀硝酸中,CuO、Cu与稀硝酸反应,生成铜盐,铜丝变红,铜丝质量减少,故C错误;
D.铜丝灼烧成黑色,加入氢氧化钠溶液不反应,质量较反应前大,故D错误.
故选B.
点评 本题考查铜及其化合物的性质,为高频考点,把握发生的反应及现象分析为解答的关键,注意Cu的质量变化,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
 A、B、C、D为中学化学中常见的烃的含氧衍生物,他们有如图的转化关系:则下列判断正确的是( )
A、B、C、D为中学化学中常见的烃的含氧衍生物,他们有如图的转化关系:则下列判断正确的是( )| A. | C→A的反应类型为加成反应 | |
| B. | 若A为2-丙醇,则其可实现如右图的所有转化 | |
| C. | 若A、B、D、为链状化合物,则C也一定为链状化合物 | |
| D. | A的相对分子质量小于C、D的相对分子质量而大于B的相对分子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

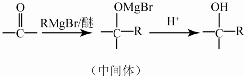
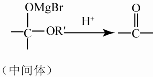
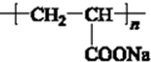

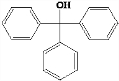 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.4g乙醛分子中含有的共用电子对数为0.6NA | |
| B. | 标准状况下,11.2L二氯甲烷所含分子数为0.5NA | |
| C. | 15.6g苯中含有碳碳双键的个数为0.6NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
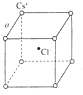 如右图是氯化铯晶体的晶胞示意图(晶体中最小的重复结构单元),已知晶体中2个最近的Cs+核间距为acm,氯化铯(CsCl)的相对分子质量M,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )
如右图是氯化铯晶体的晶胞示意图(晶体中最小的重复结构单元),已知晶体中2个最近的Cs+核间距为acm,氯化铯(CsCl)的相对分子质量M,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )| A. | $\frac{8M}{{N}_{A}{a}^{3}}$g•cm-3 | B. | $\frac{M{a}^{3}}{{8N}_{A}}$g•cm-3 | C. | $\frac{M}{{N}_{A}{a}^{3}}$g•cm-3 | D. | $\frac{M{a}^{3}}{{N}_{A}}$g•cm-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①和② | B. | ②和③ | C. | ①和③ | D. | ②和④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 粒子 | Cu2+ | Fe2+ | Fe3+ |
| 开始沉淀时的pH | 4.7 | 5.8 | 1.9 |
| 完全沉淀时的pH | 6.7 | 9.0 | 3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
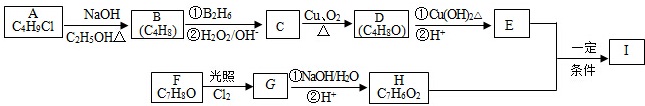
 +2Cl2$\stackrel{光照}{→}$
+2Cl2$\stackrel{光照}{→}$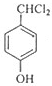 +2HCl,该反应类型为取代反应.
+2HCl,该反应类型为取代反应. .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com