
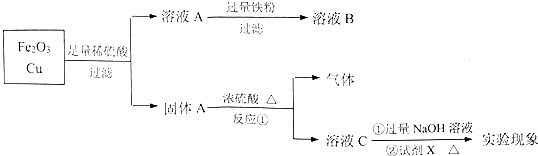
分析 氧化铁和铜的混合物加入足量稀硫酸溶解后过滤,氧化铁和硫酸反应生成硫酸铁和水,铜不反应,得到溶液A为硫酸铁溶液,硫酸铁溶液和铜反应生成硫酸亚铁和硫酸铜,固体A为Cu,与浓硫酸加热反应生成二氧化硫气体,溶液C为硫酸铜,加入过量氢氧化钠溶液反应生成氢氧化铜悬浊液,X是淀粉水解的最终产物为葡萄糖,加热葡萄糖和氢氧化铜悬浊液反应生成氧化亚铜红色沉淀,溶液A为硫酸亚铁和硫酸溶液,加入足量铁粉过滤得到溶液B为硫酸亚铁溶液,
(1)X是淀粉水解的最终产物为葡萄糖,在氢氧化铜悬浊液中加热后的实验现象是生成红色沉淀;
(2)反应①的反应为铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水;
(3)检验溶液B中阳离子为亚铁离子,检验方法为:加入KSCN 溶液,无红色出现,入通氯气溶液变红色.
解答 解:(1)X是淀粉水解的最终产物为葡萄糖,在氢氧化铜悬浊液中加热后反应,葡萄糖被氧化为葡萄糖酸,氢氧化铜悬浊液被还原为氧化亚铜,反应的实验现象是生成红色沉淀,
故答案为:产生砖红色的沉淀;
(2)反应①的反应为铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(3)检验溶液B中阳离子为亚铁离子,检验方法为:加入KSCN 溶液,无红色出现,入通氯气溶液变红色,检验溶液B中阳离子的实验步骤、现象及结论:取溶液B少量于试管中,先加入KSCN溶液不显红色,再通入Cl2,溶液变红,证明溶液B中含有Fe2+,
故答案为:取溶液B少量于试管中,先加入KSCN溶液不显红色,再通入Cl2,溶液变红,证明溶液B中含有Fe2+.
点评 本题考查了物质分离提纯、物质性质、离子检验等知识点,掌握基础是解题关键,题目难度不大.


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①>②>③>④ | B. | ④>①>②>③ | C. | ②>①=③>④ | D. | ①>②=③>④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在密闭容器中充入1 mol N2和3 mol H2,充分反应后生成NH3的分子数目为2NA | |
| B. | 标准状况下,44.8 L氮气所含的共用电子对数目为2NA | |
| C. | 常温常压下,1 mol NaHSO4固体中含有的离子数目为2NA | |
| D. | 1 mol Fe与71 g Cl2充分反应后转移的电子数目为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com