
| 实验操作 | 实验现象 | 结论或推论 | |
| A | 溴水中加入甲苯,振荡 | 水层几乎呈无色 | 甲苯与溴发生了反应 |
| B | 一小粒金属钠投入无水乙醇中 | 最后钠浮在液面上 | 密度:乙醇大于钠 |
| C | Fe(SCN)3溶液中滴入足量NaOH溶液 | 澄清后得到无色溶液 | Fe(OH)3悬浊液中滴加KSCN溶液后不显红色 |
| D | 在含Mn2+的草酸溶液中滴加酸性高锰酸钾溶液 | 高锰酸钾溶液褪色较快 | 反应过程中,Mn2+一定氧化了草酸 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.溴水与甲苯不反应,溴易溶于甲苯;
B.钠的密度比乙醇大(密度:乙醇0.79 g/mL,Na 0.97 g/cm3);
C.Fe(OH)3溶解度小,不能被SCN-检出;
D.Mn2+起到催化作用.
解答 解:A.甲苯萃取了溴,水层颜色变浅,但甲苯没有与溴发生反应,故A错误;
B.Na与乙醇反应,最后Na外面被H2包裹,整体密度小于乙醇而浮在液面上,并不能说明乙醇的密度比Na大(密度:乙醇0.79 g/mL,Na 0.97 g/cm3),故B错误;
C.Fe(SCN)3红色溶液中存在平衡,加入足量NaOH溶液与Fe3+完全反应生成Fe(OH)3沉淀,澄清后溶液呈无色,说明Fe(OH)3悬浊液中的Fe3+浓度很小(≈10-17mol/L),不能被SCN-检出,故C正确;
D.高锰酸钾溶液褪色较快的原因是Mn2+对草酸与酸性高锰酸钾溶液反应的催化作用,不是Mn2+氧化草酸,故D错误.
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及离子检验、物质的性质等知识,把握反应原理及实验技能为解答的关键,侧重分析与实验能力的考查,注意实验评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
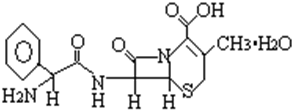 得重感冒之后,常吃一种抗生素--头孢氨苄,分子式为C16H17N3O4S•H2O,其化学结构式如图,有关其说法正确的是( )
得重感冒之后,常吃一种抗生素--头孢氨苄,分子式为C16H17N3O4S•H2O,其化学结构式如图,有关其说法正确的是( )| A. | 在一定条件下,能发生水解反应生成氨基酸 | |
| B. | 1mol该分子最多能与7molH2反应 | |
| C. | 该分子能与碳酸钠反应,不能与盐酸反应 | |
| D. | 头孢氨苄易溶于水,能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
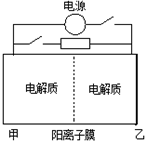 如图是一种蓄电池的示意图.被膜隔开的电解质分别为Na2S2和 NaBr3,放电后变为Na2S4和NaBr.已知放电时Na+ 由乙池向甲池移动.下面对该装置工作过程中叙述正确的是( )
如图是一种蓄电池的示意图.被膜隔开的电解质分别为Na2S2和 NaBr3,放电后变为Na2S4和NaBr.已知放电时Na+ 由乙池向甲池移动.下面对该装置工作过程中叙述正确的是( )| A. | 放电过程,甲池发生氧化反应 | |
| B. | 放电过程,电池反应:2S22-+Br3-=S42-+3Br- | |
| C. | 充电过程,乙池为阳极室 | |
| D. | 充电过程,当阳极室阴离子增加了2mol,整个电路中电子转移2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W>Z>Y | |
| B. | Y形成的离子与Z形成的离子的电子数可能相同 | |
| C. | 化合物ZY、WY3 中化学键的类型相同 | |
| D. | 由X、Y、Z、W组成的化合物的水溶液不可能显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制造普通玻璃的原料是纯碱、石灰石和石英 | |
| B. | 以粮食为原料酿酒过程的变化包括粮食→淀粉→葡萄糖→乙醇 | |
| C. | 二氧化硫有漂白性,可以使蓝色石蕊试纸褪色 | |
| D. | 漂白精、臭氧和活性炭都能用于游泳池的消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 棉布、羊毛和涤纶燃烧后都只生成二氧化碳和水 | |
| B. | 乙酸乙酯和食用植物油均可水解生成乙醇 | |
| C. | 氢氧化铝、氢氧化钠、碳酸钠都是常见的胃酸中和剂 | |
| D. | 生物柴油和石化柴油相比,使用生物柴油环保,可以减少SO2的排放,且生物柴油属于可再生能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 侯氏制碱法 | 人工合成胰岛素 | 用青蒿素治疗疟疾 | 独创无氰电镀新工艺 |
 |  |  |  |
| A.以NH3、CO2、NaCl为原料最终制得纯碱 | B.由有机小分子合成有机高分子 | C.用萃取原理从青蒿素中提取青蒿素 | D.以铜盐、碱等溶液为电解质镀铜 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=7的溶液中:Ba2+、K+、CO32-、NO3- | |
| B. | 0.1 mol•L-1NaHCO3溶液中:K+、NH4+、Cl-、SO42- | |
| C. | 0.1 mol•L-1FeCl3溶液中:Al3+、Cu2+、Br-、I- | |
| D. | 由水电离产生的c(H+)=1×10-13的溶液中:Na+、Mg2+、Cl-、HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com