
沼气是一种能源,它的主要成分是CH4。0.5mol CH4完全燃烧生成CO2和H2O(l),放出445 kJ热量,则下列热化学方程式中正确的是
A.2CH4(g) + 4O2(g) == 2CO2(g) + 4H2O(l) ΔH == +890 kJ·mol-1
B.CH4(g) + 2O2(g) == CO2(g) +2H2O(l) ΔH == +890 kJ·mol-1
C.CH4(g) + 2O2(g) == CO2(g) + 2H2O(l) ΔH == -890 kJ·mol-1
D.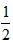 CH4(g) + O2(g) ==
CH4(g) + O2(g) == 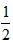 CO2(g) +H2O(l) ΔH == -890 kJ·mol-1
CO2(g) +H2O(l) ΔH == -890 kJ·mol-1
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源:2016届甘肃省张掖市高三上学期第一次质量检测化学试卷(解析版) 题型:选择题
下列实验操作一定能够达到目的的是
A.向某溶液中滴加盐酸酸化的Ba(NO3)2溶液,有白色沉淀生成,则该溶液中一定含有
B.用饱和NaHCO3溶液除去CO2气体中混有的少量SO2
C.将产生的气体依次通过足量的溴水和澄清石灰水,检验浓H2SO4与木炭反应生成的气体产物
D.实验室制取氢气,为了加快反应速率,可向稀硫酸中滴加少量Cu(NO3)2
查看答案和解析>>
科目:高中化学 来源:2016届天津一中高三零月考化学试卷(解析版) 题型:选择题
下列图示与叙述正确的是

A.图甲表示用0.1000mol/L的NaOH溶液滴定20.00ml,0.1000mol/L的醋酸溶液得到的滴定曲线
B.图乙表示压强对可逆反应2A (g)+ B (g) 3C (g)+D (s)的影响且甲的比乙的压强大
3C (g)+D (s)的影响且甲的比乙的压强大
C.图丙表示可逆反应Fe3+(aq)+SCN—(aq) Fe(SCN)2+(aq)平衡时,物质的量浓度 [Fe(SCN) 2+]与温度T的关系,反应处于D点时,一定有V(正)>V(逆)
Fe(SCN)2+(aq)平衡时,物质的量浓度 [Fe(SCN) 2+]与温度T的关系,反应处于D点时,一定有V(正)>V(逆)
D.图丁所示装置可证明溴与苯发生取代反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二上第一半月考化学试卷(解析版) 题型:选择题
25 ℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ·mol-1、285.8 kJ·mol-1、890.3 kJ·mol-1、2 800 kJ·mol-1,则下列热化学方程式正确的是
A.C(s)+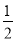 O2(g)===CO(g) ΔH=-393.5 kJ·mol-1
O2(g)===CO(g) ΔH=-393.5 kJ·mol-1
B.2H2(g)+O2(g)===2H2O(g) ΔH=+571.6 kJ·mol-1
C.CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
D.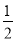 C6H12O6(s)+3O2(g)===3CO2(g)+3H2O(l) ΔH=-1 400 kJ·mol-1
C6H12O6(s)+3O2(g)===3CO2(g)+3H2O(l) ΔH=-1 400 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西太原五中高二上第一周考理科化学试卷(解析版) 题型:选择题
已知:2Zn(s) + O2(g)= 2ZnO(s) △H1= -701.0kJ·mol-1,2Hg(l)+ O2(g)= 2HgO(s) △H2= -181.6kJ·mol-1,则反应Zn(s) + HgO(s)= ZnO(s) + Hg(l)的△H为:
A.+519.4 kJ·mol-1 B.+259.7 kJ·mol-1
C.-259.7 kJ·mol-1 D.-519.4 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2016届湖南省衡阳市高三上学期第一次月考化学试卷(解析版) 题型:选择题
二氯化二硫(S2C12)是广泛用于橡胶工业的硫化剂,其分子结构如图所示。常温下,S2C12是一种橙黄色液体,遇水易水解,并产生能使品红褪色的气体,化学方程式为: 2S2C12+2H2O=SO2↑+3S↓+4HCl。下列说法中错误的是

A.S2C12的结构式为Cl—S—S—Cl
B.反应中SO2是还原产物,S是氧化产物
C.S2C12为含有极性键和非极性键的分子
D.反应中,生成1molSO2,转移电子为3mol
查看答案和解析>>
科目:高中化学 来源:2016届湖南省衡阳市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列有关物质变化和分类的说法正确的是
A.电解熔融态的Al2O3、12C转化为14C都属于化学变化
B.胆矾、冰水混合物、四氧化三铁都不是混合物
C.葡萄糖溶液和淀粉溶液的本质区别是能否发生丁达尔效应
D.SiO2、NO2、Al2O3都属于酸性氧化物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一入学摸底化学试卷(解析版) 题型:计算题
(6分)将5.1g镁铝合金投入过量盐酸中充分反应,得到500mL溶液和5.6L标准状况下的H2。计算:
(1)合金中镁和铝的质量之比;
(2)所得溶液中Mg2+的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源:2016届四川省高三9月月考化学试卷(解析版) 题型:填空题
(10分)工业合成氨与制备硝酸一般可连续生产,流程如图所示:
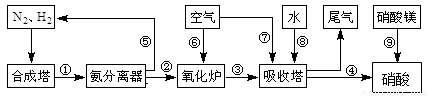
(1)工业生产时,制取氢气的一个反应为:CO+H2O(g) CO2+H2 T℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K=_____(填计算结果)。
CO2+H2 T℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K=_____(填计算结果)。
(2)合成塔中发生反应N2(g)+3H2(g) 2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1____300℃(填“>”、“<”或“=”)。
2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1____300℃(填“>”、“<”或“=”)。

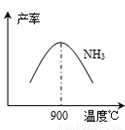
(3)N2和H2以铁作催化剂从145℃就开始反应,不同温度下NH3的产率如右图所示。温度高于900℃时,NH3产 率下降的原因是 。
率下降的原因是 。
(4)硝酸厂的尾气直接排放将污染空气,目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g); △H=-574kJ·mol-1;
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g); △H=-1160kJ·mol-1
则甲烷直接 将NO2还原为N2的热化学方程式为: 。
将NO2还原为N2的热化学方程式为: 。
(5)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极碱性条件下发生反应的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com