
用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示。下列说法正确的是
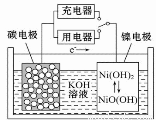
A.充电时,阴极的电极反应为:Ni(OH)2+OH--e-===NiO(OH)+H2O
B.放电时,负极的电极反应为:H2- 2e-+2OH-=== 2H2O
2e-+2OH-=== 2H2O
C.放电时,OH-移向镍电极
D.充电时,将电池的碳电极与外电源的正极相连
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年山西省高二上月考四化学卷(解析版) 题型:选择题
在一密闭容器中进行如下反应:2SO2(气)+O2(气) 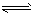 2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
A.SO2为0.4mol/L、O2为0.2mol/L B.SO2为0.25mol/L
C.SO2、SO3均为0.15mol/L D.SO3为0.4mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高二下月考二化学卷(解析版) 题型:选择题
下列各组中的两个反应所属反应类型相同的是 ( )
A.光照甲烷和氯气的混合气体,混合气体颜色变浅;乙烯能使溴水褪色
B.乙烷在氧气中燃烧;乙烯在氧气中燃烧
C.乙烯能使溴水褪色;乙烯能使酸性高锰酸钾溶液褪色
D.工业上由乙烯和水反应生成乙醇;乙烯能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一12月月考化学卷(解析版) 题型:选择题
在酸性溶液中能大量共存而且为无色透明的溶液是
A.NH4+、Al3+、SO42-、NO3- B.K+、Fe2+、NO3-、SO42-
C.K+、MnO4-、NH4+、NO3- D.Na+、K+、ClO-、NO3-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二12月月考化学卷(解析版) 题型:填空题
为减小和消除过量CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)最近有科学家提出“绿色自由”构想:先把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,并使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
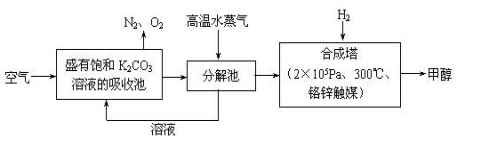
写出分解池中反应的化学方程式 。在合成塔中,当有4.4 kg CO2与足量H2完全反应 ,可放出热量4947 kJ,写出合成塔中反应的热化学方程式 。
,可放出热量4947 kJ,写出合成塔中反应的热化学方程式 。
(2)以CO2为碳源还可以制备乙醇,反应如下:
2CO2(g) + 6H2(g)=== CH3CH2OH(g) + 3H2O(g) △H=-173.6kJ/mol
写出由CH3OH(g)合成CH3CH2OH(g)的反应的热化学方程式 。
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。
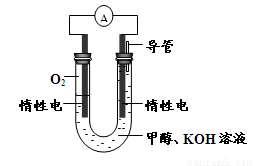
①该电池正极的电极反应为 。
②工作一段时间后,测得溶液的pH减小,该电池总反应的化学方程式为 。当电子转移 mol时,参加反应的氧气的体积是6.72L(标准状况下)。
(4)以甲醇为燃料还可制作新型燃料电池,电池的正极通入O2,负极通入甲醇,用熔融金属氧化物MO作电解质(可传导O2-)。该电池负极发生的电极反应是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二12月月考化学卷(解析版) 题型:选择题
下列离子方程式正确的是
A.AgNO3溶液中加入过量的氨水:Ag++NH3·H2O=AgOH+NH4+
B.乙酸与碳酸钠溶液反应:2CH3COOH+CO32— CO2↑+H2O+2CH3COO—
CO2↑+H2O+2CH3COO—
C.苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O— 2C6H5OH+2CO32—
2C6H5OH+2CO32—
D.用铜作电极电解氯化铜溶液:Cu2++2Cl— Cu+Cl2↑
Cu+Cl2↑
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二12月月考化学卷(解析版) 题型:选择题
下列叙述中正确的是
A.构成原电池正极和负极的材 料必须是两种金属
料必须是两种金属
B.用惰性电极电解氢氧化钠溶液,电解过程中溶液 的pH保持不变
的pH保持不变
C.马口铁(镀锡铁)破损时与电解质溶液接触锡先被腐蚀
D.蓄电池充电时,标有“+”的一端与外加电源的正极相连
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏林芝一中高一上期末化学试卷(解析版) 题型:选择题
金属材料的应用推动了社会生产力的发展。下列关于金属材料的说法,正确的是( )
A.氧化镁是一种金属材料
B.合金的硬度低于它的成分金属
C.合金分为黑色金属与有色金属
D.铁合金是目前应用范围最广的合金
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高一上期中化学卷(解析版) 题型:填空题
①VLFe2(SO4)3中含有Fe3+mg,则SO42-的物质的量浓度为____________
②6.02×1024个Na+约含_______molNa+;4.5mol甲烷约含有_________个分子,其质量为________g;
3.01×1023个CO2在标准状况下体积是________L,它与__________gCO含有相同的氧原子数。
③将4ml37%的盐酸密度为(1.19g·cm-3)加水稀释到200ml,稀释后盐酸的物质的量浓度是__________。
④在标准状况下22.4L由氮气和氧气组成给的混合气体,其质量为30g,则其中氧气的质量为__________g。
⑤同温同压下,同体积的H2和A气体的质量分别为1.0g和16.0g,则A的相对体积分子质量为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com