
分析 (1)根据n=$\frac{m}{M}$计算物质的量之比,分子数目之比等于其物质的量之比,均由氧原子构成,氧气和臭氧的质量相等,则含有氧原子数目相等;
(2)根据电子转移守恒计算金属物质的量,再根据M=$\frac{m}{n}$计算金属摩尔质量.
解答 解:(1)根据n=$\frac{m}{M}$可知,等质量的氧气和臭氧(O3)的物质的量之比为48g/mol:32g/mol=3:2,二者含有分子数目之比为3:2,均由氧原子构成,氧气和臭氧的质量相等,则含有氧原子数目相等,就所含原子数目之比为1:1,
故答案为:3:2; 3:2;1:1;
(2)生成氢气物质的量为$\frac{0.04g}{2g/mol}$=0.02mol,根据电子转移守恒,金属物质的量为$\frac{0.02mol×2}{1}$=0.04mol,则金属摩尔质量为$\frac{1.56g}{0.04mol}$=39g/mol,
故答案为:39g/mol.
点评 本题考查物质的量计算,比较基础,(2)中关键是利用电子转移守恒计算金属物质的量,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:解答题
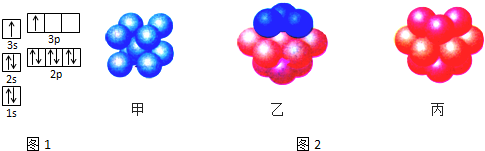
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂、热的纯碱溶液 | B. | 硫黄、CS2 | ||
| C. | 水垢、食醋 | D. | 石蜡、蒸馏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
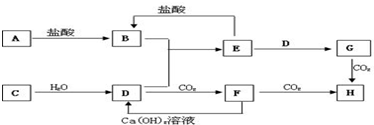
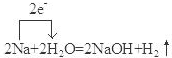 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molNa2SO4溶于水中,所得溶液中Na+个数为NA | |
| B. | 1molCO2和NO2的混合物中含的氧原子数为4NA | |
| C. | 标准状况下,NA个CCl4分子所占的体积约为22.4L | |
| D. | 54g H2O中含有3NA个水分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原试管有4mL NO2 | B. | 6mL气体全部是N2 | ||
| C. | 原试管有6mL NO2 | D. | 剩余6mL气体是NO和N2的混合气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com