
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 容量瓶不可以用来溶解固体,但可以用来稀释浓的溶液 | |
| B. | 粗盐提纯时过滤所用普通漏斗与萃取所用分液漏斗结构是一样的 | |
| C. | 用50mL量筒可准确配制50mL0.10mol/L的碳酸钠溶液 | |
| D. | 实验室制蒸馏水时冷凝管要“下进水、上出水”并保还水的持续流动 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
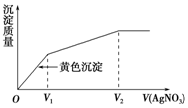 往含I-和Cl-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.则原溶液中$\frac{c({I}^{-})}{c(C{l}^{-})}$的比值为( )
往含I-和Cl-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.则原溶液中$\frac{c({I}^{-})}{c(C{l}^{-})}$的比值为( )| A. | V2-V1 | B. | $\frac{{V}_{1}}{{V}_{2}-{V}_{1}}$ | C. | $\frac{{V}_{1}}{{V}_{2}}$ | D. | $\frac{{V}_{2}}{{V}_{1}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15mL 1.5 mol•L-1的AgNO3溶液 | B. | 10mL 2 mol•L-1的NaCl溶液 | ||
| C. | 5mL 1 mol•L-1的AlCl3溶液 | D. | 5mL 1.6mol•L-1的BaCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com