
| A. | 0.1 mol/L NaB溶液中水电离的OH-浓度大于10-7 mol/L | |
| B. | NaB溶液中:c(Na+)>c(B-)>c(H+)>c(OH-) | |
| C. | NaB溶液中:c(Na+)+c(H+)=c(HB)+c(B-) | |
| D. | HB的电离方程式为:HB═H++B- |
分析 某一元酸(HB)的盐NaB的水溶液呈碱性,说明NaB为强碱弱酸盐,则HB为弱酸,NaB可促进水的电离,结合溶液电荷守恒解答该题.
解答 解:A.酸或碱抑制水电离,含有弱离子的盐促进水电离,NaB为强碱弱酸盐,所以0.1mol/L NaB溶液中水电离的OH-浓度大于10-7mol/L,故A正确;
B.NaB为强碱弱酸盐,酸根离子在水溶液里部分电离导致溶液呈碱性,则c(H+)<c(OH-),故B错误;
C.任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)═c(OH-)+c(B-),因为水也电离生成氢氧根离子,所以c(OH-)>c(HB),则c(Na+)+c(H+)>c(HB)+c(B-),故C错误;
D.HB为弱酸,在水溶液里部分电离,电离方程式为HB?H++B-,故D错误.
故选A.
点评 本题考查弱电解质的电离,为高频考点,侧重考查学生的分析能力,注意根据盐溶液酸碱性确定酸的强弱,灵活运用守恒思想分析解答,注意C选项,为易错点.


科目:高中化学 来源: 题型:推断题
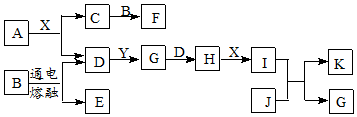
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=+110.5 kJ•mol-1 | |
| B. | C(s)+O2(g)═CO2(g)△H=-393.5 kJ•mol-1 | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1 | |
| D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
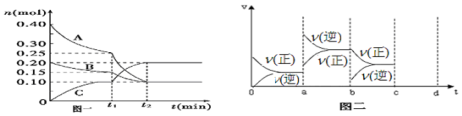
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol固态物质或液态物质的体积主要决定于构成这种物质的粒子的大小和粒子数目 | |
| B. | 在相同温度和压强下,任何气体粒子之间的距离可看成相等的 | |
| C. | 配制一定物质的量浓度的硫酸溶液时,用量筒量取一定体积的浓硫酸倒入烧杯后,再用蒸馏水洗涤量筒2~3次,并将洗涤液一并倒入烧杯中稀释 | |
| D. | 为与容量瓶的精度相匹配称量固体质量时不应用托盘天平 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na在空气中长期放置最终变为Na2CO3粉末 | |
| B. | Na2O 和Na2O2都能与水反应生成碱,它们都是碱性氧化物 | |
| C. | 铝与氢氧化钠的反应中水和氢氧化钠均作氧化剂 | |
| D. | 铝箔在空气中受热可以熔化,且发生剧烈燃烧 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com