
| c£ØX£©/mol?L-1 ČŻĘ÷Ģå»ż/L ĪĀ¶Č/”ę |
1 | 2 | 3 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
| A”¢m£¾n |
| B”¢ĪĀ¶Č²»±ä£¬Ōö“óĢå»ż£¬XµÄ×Ŗ»ÆĀŹŌö“ó |
| C”¢Q£¼0 |
| D”¢Ģå»ż²»±ä£¬ĪĀ¶ČÉżøߣ¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ |
| 1 |
| 2 |
| 1 |
| 2 |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
(15·Ö)¼×“¼æÉĶعż½«ĆŗµÄĘų»Æ¹ż³ĢÖŠÉś³ÉµÄCOŗĶH2ŌŚŅ»¶ØĢõ¼žĻĀ£¬·¢ÉśČēĻĀ·“Ó¦ÖĘµĆ£ŗ”£Ēėøł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£ŗ
(1) “Ó·“Ó¦æŖŹ¼µ½Ę½ŗā£¬ÓĆCOÅØ¶Č±ä»Æ±ķŹ¾Ę½¾ł·“Ó¦ĖŁĀŹv(CO)=________”£
(2) Š“³öøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½________________
(3) ŗćČŻĢõ¼žĻĀ,ĻĀĮŠ“ėŹ©ÖŠÄÜŹ¹Ōö“óµÄÓŠ________________
AÉżøßĪĀ¶Č B³äČĖHeĘų
CŌŁ³äČė1molCOŗĶ2mol H2 DŹ¹ÓĆ“ß»Æ¼Į
(4) ČōŌŚĪĀ¶ČŗĶČŻĘ÷ĻąĶ¬µÄČżøöĆܱÕČŻĘ÷ÖŠ,°“²»Ķ¬·½Ź½Ķ¶ČĖ·“Ó¦Īļ.£¬²āµĆ·“Ó¦“ļµ½Ę½ŗā ¼µÄÓŠ¹ŲŹż¾ŻČēĻĀ±ķ£ŗ
ŌņĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ________
A c1=c2 B.
C. 2a1=a3 D. a1 +a2 =1
EøĆ·“Ó¦ČōÉś³É1molCH3OH£¬Ōņ·Å³ö(Q1+Q2)kJČČĮæ
(5) ČōŌŚŅ»Ģå»żæɱäµÄĆܱÕČŻĘ÷ÖŠ³äČėl mol CO 2mol H2ŗĶ1mol CH3OH£¬“ļµ½Ę½ŗā ¼²āµĆ»ģŗĻĘųĢåµÄĆܶȏĒĶ¬ĪĀĶ¬Ń¹ĻĀĘšŹ¼µÄ1.6±¶£¬ŌņøĆ·“Ó¦Ļņ________(Ģī”°Õż”±”¢”°Äę”±)·“Ó¦·½ĻņŅĘ¶Æ£¬ĄķÓÉŹĒ________________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2012-2013ѧğŗÓÄĻŹ”°²ŃōŅ»ÖŠø߶žµŚ¶ž“Ī½×¶Īæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø“ų½āĪö£© ĢāŠĶ£ŗĢīæÕĢā
£Ø19·Ö£©ĪŅ¹ś”¶³µÓĆČ¼ĮĻ¼×“¼¹ś¼Ņ±ź×¼”·µÄŹµŹ©ĄæŖĮĖ³µÓĆČ¼ĮĻµĶĢ¼øļĆüµÄ“óÄ»£¬Ņ»Š©Ź”ŹŠÕżŌŚĀ½ŠųŹŌµćÓėĶĘ¹ćŹ¹ÓĆ¼×“¼ĘūÓĶ”£¼×“¼æÉĶعż½«ĆŗµÄĘų»Æ¹ż³ĢÖŠÉś³ÉµÄCOŗĶH2ŌŚŅ»¶ØĢõ¼žĻĀ·¢ÉśČēĻĀ·“Ó¦ÖĘµĆ£ŗCO(g) + 2H2(g)  CH3OH(g)”£Ķ¼I”¢Ķ¼¢ņŹĒ¹ŲÓŚøĆ·“Ó¦½ųŠŠĒéæöµÄĶ¼Ź¾”£
CH3OH(g)”£Ķ¼I”¢Ķ¼¢ņŹĒ¹ŲÓŚøĆ·“Ó¦½ųŠŠĒéæöµÄĶ¼Ź¾”£
Ēėøł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Ķ¼IŹĒ·“Ó¦Ź±COŗĶCH3OHµÄÅضČĖꏱ¼äµÄ±ä»ÆĒéæö£¬“Ó·“Ó¦æŖŹ¼µ½Ę½ŗā£¬ÓĆCOÅØ¶Č±ä»Æ±ķŹ¾Ę½¾ł·“Ó¦ĖŁĀŹv(CO)=_______________”£
£Ø2£©Ķ¼¢ņ±ķŹ¾øĆ·“Ó¦½ųŠŠ¹ż³ĢÖŠÄÜĮæµÄ±ä»Æ£¬ĒśĻßa±ķŹ¾²»Ź¹ÓĆ“ß»Æ¼ĮŹ±·“Ó¦µÄÄÜĮæ±ä»Æ£¬ŌŚĶ¼¢ņÖŠ»³öŹ¹ÓĆ“ß»Æ¼ĮŗóµÄÄÜĮæ±ä»ÆĒśĻßb”£
£Ø3£©Š“³öøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ ”£
£Ø4£©øĆ·“Ó¦µÄĘ½ŗā³£ŹżKµÄ±ķ“ļŹ½ĪŖ £»µ±ĪĀ¶ČÉżøߏ±£¬øĆĘ½ŗā³£ŹżK½«________£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©”£
£Ø5£©ŗćČŻĢõ¼žĻĀ£¬ĻĀĮŠ“ėŹ©ÖŠÄÜŹ¹ Ōö“óµÄÓŠ ”£
Ōö“óµÄÓŠ ”£
A£®ÉżøßĪĀ¶Č B£®³äČĖHeĘų
C£®ŌŁ³äČė1molCOŗĶ2molH2 D£®Ź¹ÓĆ“ß»Æ¼Į
£Ø6£©ŌŚŗćĪĀĢõ¼žĻĀ£¬±£³ÖCOÅØ¶Č²»±ä£¬Ą©“óČŻĘ÷Ģå»ż£¬ŌņĘ½ŗā £ØĢī”°ÄęĻņŅĘ¶Æ”±”¢”°ÕżĻņŅĘ¶Æ”±”¢”°²»ŅĘ¶Æ”±£©
£Ø7£©ŌŚĪĀ¶Č”¢ČŻ»żĻąĶ¬µÄČżøöĆܱÕČŻĘ÷ÖŠ£¬°“²»Ķ¬·½Ź½Ķ¶ĮĻ£¬±£³ÖŗćĪĀ”¢ŗćČŻ£¬²āµĆ·“Ó¦“ļµ½Ę½ŗāŹ±µÄÓŠ¹ŲŹż¾ŻČēĻĀ
| ČŻĘ÷ | ¼× | ŅŅ | ±ū |
| Ķ¶ĮĻĮæ | 1mol CO ”¢2mol H2 | 1molCH3OH | 2molCH3OH |
| CH3OHµÄÅØ¶Č£Ømol”¤L-1£© | c1 | c2 | c3 |
| ·“Ó¦µÄÄÜĮæ±ä»Æ | ·Å³öQ1kJ | ĪüŹÕQ2kJ | ĪüŹÕQ3kJ |
| ĢåĻµŃ¹Ēæ£ØPa£© | P1 | P2 | P3 |
| ·“Ó¦Īļ×Ŗ»ÆĀŹ | ¦Į1 | ¦Į2 | ¦Į3 |
 E£®2¦Į2=¦Į3
E£®2¦Į2=¦Į3²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2012½ģ¹óÖŻŹ”äŲĢ¶ÖŠŃ§øßČżµŚĪå“ĪŌĀæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢīæÕĢā
(15·Ö)¼×“¼æÉĶعż½«ĆŗµÄĘų»Æ¹ż³ĢÖŠÉś³ÉµÄCOŗĶH2ŌŚŅ»¶ØĢõ¼žĻĀ£¬·¢ÉśČēĻĀ·“Ó¦ÖĘµĆ£ŗ ”£Ēėøł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£ŗ
”£Ēėøł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£ŗ
(1) “Ó·“Ó¦æŖŹ¼µ½Ę½ŗā£¬ÓĆCOÅØ¶Č±ä»Æ±ķŹ¾Ę½¾ł·“Ó¦ĖŁĀŹv(CO)=________”£
(2) Š“³öøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½________________
(3) ŗćČŻĢõ¼žĻĀ,ĻĀĮŠ“ėŹ©ÖŠÄÜŹ¹ Ōö“óµÄÓŠ________________
Ōö“óµÄÓŠ________________
AÉżøßĪĀ¶Č B³äČĖHeĘų
CŌŁ³äČė1molCOŗĶ2mol H 2 DŹ¹ÓĆ“ß»Æ¼Į
(4) ČōŌŚĪĀ¶ČŗĶČŻĘ÷ĻąĶ¬µÄČżøöĆܱÕČŻĘ÷ÖŠ,°“²»Ķ¬·½Ź½Ķ¶ČĖ·“Ó¦Īļ.£¬²āµĆ·“Ó¦“ļµ½Ę½ŗā
¼µÄÓŠ¹ŲŹż¾ŻČēĻĀ±ķ£ŗ
ŌņĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ________
A c1=c2 B. 
C. 2a1=a3 D. a1 +a2 =1
EøĆ·“Ó¦ČōÉś³É1mol CH3OH£¬Ōņ·Å³ö(Q1+Q2)kJČČĮæ
(5) ČōŌŚŅ»Ģå»żæɱäµÄĆܱÕČŻĘ÷ÖŠ³äČėl mol CO 2mol H2ŗĶ1mol CH3OH£¬“ļµ½Ę½ŗā
¼²āµĆ»ģŗĻĘųĢåµÄĆܶȏĒĶ¬ĪĀĶ¬Ń¹ĻĀĘšŹ¼µÄ1.6±¶£¬ŌņøĆ·“Ó¦Ļņ________(Ģī”°Õż”±”¢”°Äę”±)·“Ó¦·½ĻņŅĘ¶Æ£¬ĄķÓÉŹĒ________________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014½ģŗÓÄĻŹ”ø߶žµŚ¶ž“Ī½×¶Īæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø19·Ö£©ĪŅ¹ś”¶³µÓĆČ¼ĮĻ¼×“¼¹ś¼Ņ±ź×¼”·µÄŹµŹ©ĄæŖĮĖ³µÓĆČ¼ĮĻµĶĢ¼øļĆüµÄ“óÄ»£¬Ņ»Š©Ź”ŹŠÕżŌŚĀ½ŠųŹŌµćÓėĶĘ¹ćŹ¹ÓĆ¼×“¼ĘūÓĶ”£¼×“¼æÉĶعż½«ĆŗµÄĘų»Æ¹ż³ĢÖŠÉś³ÉµÄCOŗĶH2ŌŚŅ»¶ØĢõ¼žĻĀ·¢ÉśČēĻĀ·“Ó¦ÖĘµĆ£ŗCO(g) + 2H2(g)  CH3OH(g)”£Ķ¼I”¢Ķ¼¢ņŹĒ¹ŲÓŚøĆ·“Ó¦½ųŠŠĒéæöµÄĶ¼Ź¾”£
CH3OH(g)”£Ķ¼I”¢Ķ¼¢ņŹĒ¹ŲÓŚøĆ·“Ó¦½ųŠŠĒéæöµÄĶ¼Ź¾”£

Ēėøł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Ķ¼IŹĒ·“Ó¦Ź±COŗĶCH3OHµÄÅضČĖꏱ¼äµÄ±ä»ÆĒéæö£¬“Ó·“Ó¦æŖŹ¼µ½Ę½ŗā£¬ÓĆCOÅØ¶Č±ä»Æ±ķŹ¾Ę½¾ł·“Ó¦ĖŁĀŹv(CO)=_______________”£
£Ø2£©Ķ¼¢ņ±ķŹ¾øĆ·“Ó¦½ųŠŠ¹ż³ĢÖŠÄÜĮæµÄ±ä»Æ£¬ĒśĻßa±ķŹ¾²»Ź¹ÓĆ“ß»Æ¼ĮŹ±·“Ó¦µÄÄÜĮæ±ä»Æ£¬ŌŚĶ¼¢ņÖŠ»³öŹ¹ÓĆ“ß»Æ¼ĮŗóµÄÄÜĮæ±ä»ÆĒśĻßb”£
£Ø3£©Š“³öøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ ”£
£Ø4£©øĆ·“Ó¦µÄĘ½ŗā³£ŹżKµÄ±ķ“ļŹ½ĪŖ £»µ±ĪĀ¶ČÉżøߏ±£¬øĆĘ½ŗā³£ŹżK½«________£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©”£
£Ø5£©ŗćČŻĢõ¼žĻĀ£¬ĻĀĮŠ“ėŹ©ÖŠÄÜŹ¹ Ōö“óµÄÓŠ
ӣ
Ōö“óµÄÓŠ
ӣ
A£®ÉżøßĪĀ¶Č B£®³äČĖHeĘų
C£®ŌŁ³äČė1molCOŗĶ2molH2 D£®Ź¹ÓĆ“ß»Æ¼Į
£Ø6£©ŌŚŗćĪĀĢõ¼žĻĀ£¬±£³ÖCOÅØ¶Č²»±ä£¬Ą©“óČŻĘ÷Ģå»ż£¬ŌņĘ½ŗā £ØĢī”°ÄęĻņŅĘ¶Æ”±”¢”°ÕżĻņŅĘ¶Æ”±”¢”°²»ŅĘ¶Æ”±£©
£Ø7£©ŌŚĪĀ¶Č”¢ČŻ»żĻąĶ¬µÄČżøöĆܱÕČŻĘ÷ÖŠ£¬°“²»Ķ¬·½Ź½Ķ¶ĮĻ£¬±£³ÖŗćĪĀ”¢ŗćČŻ£¬²āµĆ·“Ó¦“ļµ½Ę½ŗāŹ±µÄÓŠ¹ŲŹż¾ŻČēĻĀ
|
ČŻĘ÷ |
¼× |
ŅŅ |
±ū |
|
Ķ¶ĮĻĮæ |
1mol CO Ӣ2mol H2 |
1molCH3OH |
2molCH3OH |
|
CH3OHµÄÅØ¶Č£Ømol”¤L-1£© |
c1 |
c2 |
c3 |
|
·“Ó¦µÄÄÜĮæ±ä»Æ |
·Å³öQ1 kJ |
ĪüŹÕQ2 kJ |
ĪüŹÕQ3 kJ |
|
ĢåĻµŃ¹Ēæ£ØPa£© |
P1 |
P2 |
P3 |
|
·“Ó¦Īļ×Ŗ»ÆĀŹ |
¦Į1 |
¦Į2 |
¦Į3 |
ŌņĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ
A£®c1= c2 B£®Q3 = 2Q2 C£®2 P1£¼P3
D£®¦Į1+¦Į2=1 E£®2¦Į2=¦Į3
E£®2¦Į2=¦Į3
F£®øĆ·“Ó¦ČōÉś³É1molCH3OH·Å³öµÄČČĮæĪŖ£ØQ1+ Q2£©kJ
£Ø8£©ČōŌŚŅ»Ģå»żæɱäµÄĆܱÕČŻĘ÷ÖŠ³äČė1mol CO”¢2mol H2ŗĶ1molCH3OH£¬“ļµ½Ę½ŗāŹ±²āµĆ»ģŗĻĘųĢåµÄĆܶȏĒĶ¬ĪĀĶ¬Ń¹ĻĀĘšŹ¼µÄ1.6±¶£¬ŌņøĆ·“Ó¦Ļņ £ØĢī”°Õż”±”¢”°Äę”±£©·“Ó¦·½ĻņŅĘ¶Æ£¬ĄķÓÉŹĒ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2011-2012ѧğ¹óÖŻŹ”øßČżµŚĪå“ĪŌĀæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢīæÕĢā
(15·Ö)¼×“¼æÉĶعż½«ĆŗµÄĘų»Æ¹ż³ĢÖŠÉś³ÉµÄCOŗĶH2ŌŚŅ»¶ØĢõ¼žĻĀ£¬·¢ÉśČēĻĀ·“Ó¦ÖĘµĆ£ŗ ”£Ēėøł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£ŗ
”£Ēėøł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£ŗ

(1) “Ó·“Ó¦æŖŹ¼µ½Ę½ŗā£¬ÓĆCOÅØ¶Č±ä»Æ±ķŹ¾Ę½¾ł·“Ó¦ĖŁĀŹv(CO)=________”£
(2) Š“³öøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½________________
(3) ŗćČŻĢõ¼žĻĀ,ĻĀĮŠ“ėŹ©ÖŠÄÜŹ¹ Ōö“óµÄÓŠ________________
Ōö“óµÄÓŠ________________
AÉżøßĪĀ¶Č B³äČĖHeĘų
CŌŁ³äČė1molCOŗĶ2mol H 2 DŹ¹ÓĆ“ß»Æ¼Į
(4) ČōŌŚĪĀ¶ČŗĶČŻĘ÷ĻąĶ¬µÄČżøöĆܱÕČŻĘ÷ÖŠ,°“²»Ķ¬·½Ź½Ķ¶ČĖ·“Ó¦Īļ.£¬²āµĆ·“Ó¦“ļµ½Ę½ŗā ¼µÄÓŠ¹ŲŹż¾ŻČēĻĀ±ķ£ŗ
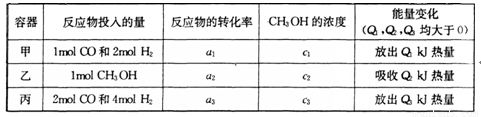
ŌņĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ________
A c1=c2 B. 
C. 2a1=a3 D. a1 +a2 =1
EøĆ·“Ó¦ČōÉś³É1mol CH3OH£¬Ōņ·Å³ö(Q1+Q2)kJČČĮæ
(5) ČōŌŚŅ»Ģå»żæɱäµÄĆܱÕČŻĘ÷ÖŠ³äČėl mol CO 2mol H2ŗĶ1mol CH3OH£¬“ļµ½Ę½ŗā ¼²āµĆ»ģŗĻĘųĢåµÄĆܶȏĒĶ¬ĪĀĶ¬Ń¹ĻĀĘšŹ¼µÄ1.6±¶£¬ŌņøĆ·“Ó¦Ļņ________(Ģī”°Õż”±”¢”°Äę”±)·“Ó¦·½ĻņŅĘ¶Æ£¬ĄķÓÉŹĒ________________
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com