
常温下,在pH为3的FeCl3溶液、pH为11的Na2CO3溶液和pH为3的盐酸中,由水电离出来的H+的浓度分别为c1、c2、c3,它们之间的关系是
A.c1<c2<c3 B.c1=c2>c3 C.c1>c2>c3 D.无法判断
科目:高中化学 来源:2016-2017学年西藏拉萨中学高二上期末化学试卷(解析版) 题型:选择题
2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200 oC左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:C2H5OH +3O2 =2CO2 +3H2O, 电池示意如右图,下列说法不正确的是:
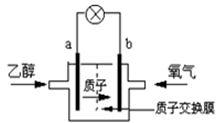
A.b极为电池的正极
B.电池正极的电极反应为:4H+ + O2 + 4e- =2H2O
C.电 池工作时电子由b极沿导线经灯泡再到a极
池工作时电子由b极沿导线经灯泡再到a极
D.电池工作时,1mol乙醇被氧化时就有12mol电子转移
查看答案和解析>>
科目:高中化学 来源:2016-2017年陕西西藏民族学院附中高二12月月考化学卷(解析版) 题型:选择题
室溫下,向0.1 mol/L氨水中逐滴加入盐酸,下列描述不正确的是
A.pH逐渐减小 B.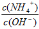 增大
增大
C.水的电离程度会不断增大 D.Kw不变
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西西安一中高二上月考二化学卷(解析版) 题型:选择题
用两根铂丝作电极插入KOH溶液中,再分别向两极通入甲烷气体和氧气,可形成燃料电池,该电池放电时的总反应为:CH4+2KOH+2O2═K2CO3+3H2O,下列说法错误的是( )
A. 放电一段时间后,KOH的物质的量不发生变化
B. 放电时通入氧气的一极附近溶液的pH升高
C. 通甲烷的一极为负极,通氧气的一极为正极
D. 通甲烷的电极反应式是:CH4+10OH--8e-═CO32-+7H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西西安一中高二上月考二化学卷(解析版) 题型:选择题
下列关于电解质溶液的叙述正确的是
A.常温下,在pH=7的醋酸钠和醋酸混合溶液中:c(CH3COO-)>c(Na+)
B.稀释醋酸溶液,溶液中所有离子的浓度均降低
C.在pH=5的氯化钠和稀硝酸的混合溶液中,c(Na+)=c(Cl-)
D.0.1 mol·L-1的硫化钠溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西西安一中高二上月考二化学卷(解析版) 题型:选择题
某学生的实验报告所列出的下列数据中合理的是
A.用10mL量筒量取7.13 mL稀盐酸
B.用托盘天平称量25.20 g NaCl
C.用广泛pH试纸测得某溶液的pH为2.3
D.用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70 mL
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上月考四化学卷(解析版) 题型:填空题
(1)常温下,如果取0.1mol•L-1HA溶液与0.1mol•L-1NaOH溶液等体积混合,测得混合液的pH=8。混合液中由水电离出的OH-浓度与0.1mol•L-1NaOH溶液中由水电离出的OH-浓度之比为__________.
(2)相同温度下,将足量硫酸钡固体分别放入相同体积的
①0.1mol•L-1硫酸铝溶液
②0.1mol•L-1氯化钡溶液
③蒸馏水
④0.1mol•L-1硫酸溶液中,
Ba2+浓度由大到小的顺序是 。(用序号填写)
(3)常温下,将a mol•L-1的氨水与0.1mol•L-1的盐酸等体积混合,当溶液中c(NH4+)=c(Cl-)时,用含a的代数式表示NH3•H2O的电离常数Kb= 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上月考四化学卷(解析版) 题型:选择题
相同温度下等物质的量浓度的下列溶液中,pH值最小的是
A.NH4Cl B.NH4HCO3 C.NH4HSO4 D.(NH4)2SO4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一12月月考化学卷(解析版) 题型:推断题
现有金属单质A、B、C、I和气体甲、乙、丙及物质D、E、F、G、H。其中B是地壳中含量最多的金属。它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
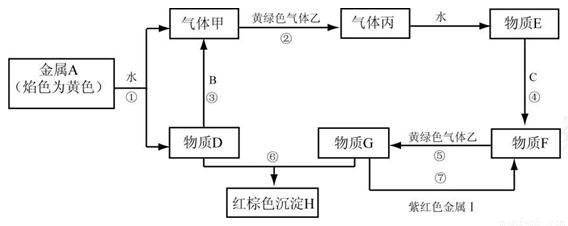
请根据以上信息回答下列问题:
(1)写出下列物质的化学式: C 、H
(2)写出反应③的化学方程式: 写出反应⑦的离子方程式:
(3)实验室检验物质G中阳离子的常用试剂是: 实验室检验物质D中阳离 子的方法是
子的方法是
(4)写出物质D溶液加入物质F溶液中反应的离子方程式 ;该物质露置空气中发生反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com