
| A. | 8种 | B. | 9种 | C. | 10种 | D. | 7种 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 如图所示的装置,C、D、E、F、X、Y都是惰性电极.接通电源后,向乙中滴入酚酞溶液,在F极附近显红色.试回答下列问题:
如图所示的装置,C、D、E、F、X、Y都是惰性电极.接通电源后,向乙中滴入酚酞溶液,在F极附近显红色.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 周 期 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 元素种类 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
| A. | 18种 | B. | 32种 | C. | 50种 | D. | 64种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4和Cl2光照发生取代反应 | |
| B. | 1,3-丁二烯与等物质的量的溴发生反应 | |
| C. | 乙烯和氯化氢加成 | |
| D. | 乙醇汽油 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
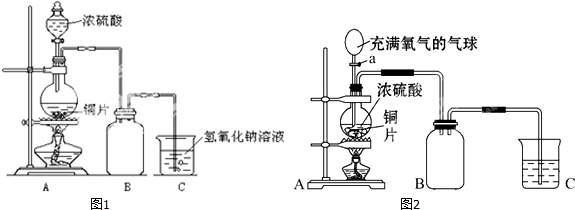
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | E(3s)>E(3p)>E(3d) | B. | E(3s)>E(2s)>E(1s) | C. | E(4f)>E(3d)>E(4s) | D. | E(5s)>E(4s)>E(4f) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
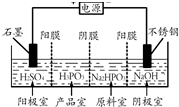 亚磷酸(H3PO3)可用作检测汞、金、银、铅、碘酸等的分析试剂.
亚磷酸(H3PO3)可用作检测汞、金、银、铅、碘酸等的分析试剂.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com