
科目:高中化学 来源: 题型:
| A、在常温下,放热反应一般能自发进行,吸热反应都不能自发进行 |
| B、因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 |
| C、NH4HCO3(s)═NH3(g)+H2O(g)+CO2(g)△H=+185.57 kJ/mol,能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
| D、在其他外界条件不变的情况下,使用催化剂可以改变化学反应进行的方向 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数定 | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
| 时间/min | N2(mol?L-1) | 02(mol?L-1) | NO(mol?L-1) |
| 0 | 2.60 | 2.60 | 0 |
| 2 | 2.54 | 2.54 | 0.12 |
| 3 | c1 | c2 | c3 |
| 4 | c1 | c2 | c3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
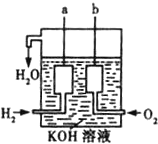 氢气燃烧生成液态水的热化学方程式是2H2(g)+O2(g)═2H2O(l);△H=-572kJ/mol请回答下列问题:
氢气燃烧生成液态水的热化学方程式是2H2(g)+O2(g)═2H2O(l);△H=-572kJ/mol请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、配位键也是一种静电作用 |
| B、配位键实质也是一种共价键 |
| C、形成配位键的电子对由成键双方原子提供 |
| D、配位键具有饱和性和方向性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com