
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A. Mg(OH)2(s)![]() MgCl2(aq)
MgCl2(aq)![]() Mg(s)
Mg(s)
B. FeCl2(aq)![]() FeCl3(aq)
FeCl3(aq)![]() Fe(OH)3(胶体)
Fe(OH)3(胶体)
C. 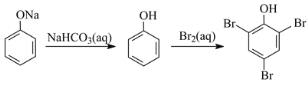
D. AgNO3(aq)![]() [Ag(NH3)2]+(aq)
[Ag(NH3)2]+(aq)![]() Ag(s)
Ag(s)
【答案】B
【解析】
A. MgCl2溶液电解不能产生金属Mg;
B. FeCl2与氯气反应产生氯化铁,氯化铁饱和溶液滴入沸水中产生氢氧化铁胶体;
C.酸性:苯酚>HCO3-;
D.蔗糖是非还原性糖。
A. 用惰性电极电解MgCl2溶液,产生Mg(OH)2、H2、Cl2,不能产生金属Mg,A错误;
B.FeCl2具有还原性,与氯气在溶液中发生氧化还原反应产生氯化铁,将氯化铁饱和溶液滴入沸水中产生氢氧化铁胶体,B正确;
C.由于苯酚的酸性比NaHCO3强,所以向苯酚钠溶液中加入NaHCO3溶液,不能发生反应产生苯酚,C错误;
D.向AgNO3溶液中滴加稀氨水,直至开始产生的沉淀恰好溶解为止,得到的溶液为银氨溶液,但由于蔗糖分子中无醛基,因此再滴入蔗糖溶液,不能发生银镜反应,D错误;
故合理选项是B。


科目:高中化学 来源: 题型:
【题目】将1.95g由Na2SO4和Na2CO3组成的混合物溶于水得溶液A,在A中加入10mL未知的BaCl2溶液恰好完全反应,过滤得沉淀B,向B中加入足量稀盐酸,充分反应后剩余沉淀2.33g。计算:
(1)原混合物中Na2SO4的物质的量___。
(2)碳酸钠的质量分数___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钕铁硼磁铁是目前为止具有最强磁力的永久磁铁。生产钕铁硼磁铁的主要原材料有稀土金属钕、高纯铁、铝、硼等。回答下列问题:
(1)钕(Nd)为60号元素,在周期表中位于第_________周期。基态硼原子中占据最高能级的电子,电子云轮廓图形状为_______。铁离子的电子排布式__________________
(2)实验测得AlCl3的实际存在形式为Al2Cl6,其分子的球棍模型如下图所示:
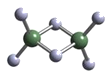
① 分子中A1原子采取____杂化。Al2Cl6属于____分子(填“极性”或“非极性”)。
②AlCl3与过量NaOH溶液反应生成Na[Al(OH)4],[A1(OH)4]-中存在的化学键有_________(填选项字母)。
A.离子键 B.共价键 C.配位键 D.金属键 E.氢键
(3)工业上可用电解熔融的FeO、Fe2O3冶炼高纯铁。基态Fe2+的价电子排布图(轨道表达式)为______________;用物质结构知识说明Fe2+容易被氧化成Fe3+的原因:________________________。
(4)氮化铁晶体的晶胞结构如图1所示。该晶体中铁、氮的微粒个数之比为_____。
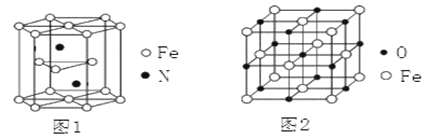
(5)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm—3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为_________;Fe2+与O2—的最短核间距为_____________pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物燃料电池(MFC)为可再生能源的开发和难降解废弃物的处理提供了一条新途径。某微生物燃料电池示意图如图所示(假设废弃物为乙酸盐)。下列说法错误的是( )

A.甲室菌为好氧菌,乙室菌为厌氧菌
B.甲室的电极反应式为![]()
C.该微生物燃料电池(MFC)电流的流向:由b经导线到a
D.电池总反应式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年2月《Nature》报道的一种四室(1#~4#)自供电从低浓度废水中回收铜等重金属的装置如下图所示:
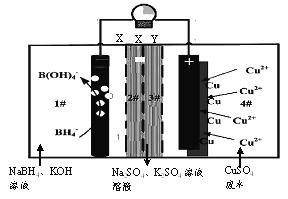
下列说法正确的是
A. 装置工作时,4#室中溶液pH不变
B. X、Y依次为阴离子、阳离子选择性交换膜
C. 负极的电极反应为:BH4-+8OH--8e-=B(OH)4-+4H2O
D. 单位时间内4n(NaBH4)消耗>n(Cu)生成是由于负极上有O2析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四种短周期元素,相关信息如下表。
元素 | 相关信息 |
A | 气态氢化物极易溶于水,可用作制冷剂 |
B | 单质的焰色反应为黄色 |
C | 单质是黄绿色气体,可用于自来水消毒 |
D | –2价阴离子的结构示意图是 |
请根据表中信息回答:
(1) A在周期表中的位置______。
(2) B与C形成化合物的类型为______(填“离子化合物”或“共价化合物”)
(3) 最高价氧化物对应的水化物的酸性C强于D,请用原子结构解释原因______。
(4) 已知硒(Se) 与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是______。
a.非金属性比D元素的强
b.SeO2既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为H2SeO4
查看答案和解析>>
科目:高中化学 来源: 题型:
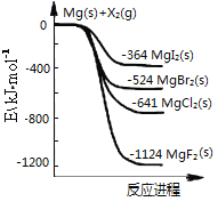
【题目】如图是金属镁和卤素单质(X2)反应的能量变化示意图。下列说法正确的是
A. 卤素单质(X2)与水反应均可生成两种酸
B. MgF2的电子式为:![]()
C. 热稳定性:MgI2>MgBr2>MgCl2>MgF2
D. 由图可知此温度下MgI2(s)与Cl2(g)反应的热化学方程式为:MgI2(s)+Cl2(g)=MgCl2(s)+I2(g) ΔH=-277 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、铬及其相关化合物用途非常广泛。回答下列问题:
(1)基态N原子的核外电子排布式为___,Cr位于元素周期表第四周期___族。
(2) Cr与K位于同一周期且最外层电子数相同,两种元素原子第一电离能的大小关系为___;Crcl3的熔点(83℃)比CrF3的熔点(1100℃)低得多,这是因为___。
(3) Cr的一种配合物结构如图所示:

①阴离子C1O4-的空间构型为___形。
②配离子中,中心离子的配位数为___,N与中心原子形成的化学键称为___键。
③配体H2 NCH2 CH2 NH2(乙二胺)中碳原子的杂化方式是______ ,分子中三种元素电负性从大到小的顺序为___
(4)氮化铬的熔点为1770℃,它的一种晶体的晶胞结构如图所示,其密度为5. 9 g·cm -3,氮化铬的晶胞边长为___(列出计算式)nm.

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com