
反应3A(g)+B(g)  2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是
2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是
A.v (A)=0.15 mol·L-1·s-1 B.v (B)=0.3 mol·L-1·s-1
C.v (C)=0.5 mol·L-1·s-1 D.v (D)=0.4 mol·L-1·s-1
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
将0.34 g Cu和CuO的混合物加入约12 mol·L-1浓硫酸中,并加热使其完全溶解,然后用NaOH溶液中和过量硫酸,再用水稀释到0.5 L,加入纯铁粉1.85 g,反应后过滤、干燥,得不溶物1.89 g。求置换出的铜的质量及原混合物中铜的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是一种试验某气体化学性质的实验装置,图中B为开关。 如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液是( )
A.浓H2SO4 B.饱和NaCl溶液 C.浓NaOH溶液 D.饱和Na2CO3

查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于浓硫酸和浓硝酸的叙述不正确的是( )
A.加热条件下均能与碳反应 B.长期露置在空气中浓度均会降低
C.常温下均不能用铁制容器贮存 D.一定条件下均可与铜片反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某小组取一定质量的FeSO4固体,利用下图装置进行实验。250mL容量瓶
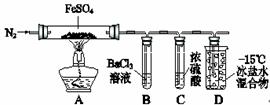
| 实验过程 | 实验现象 | |
| ① | 通入一段时间N2,加热 | A中固体变为红棕色,B中有白色沉淀,D试管中有无色液体 |
| ② | 用带有火星的木条靠近装置D的导管口 | 木条复燃 |
| ③ | 充分反应,停止加热,冷却后,取A中固体,加盐酸 | 固体溶解,溶液呈黄色 |
| ④ | 将③所得溶液滴入D试管中 | 溶液变为浅绿色 |
已知:SO2熔点–72℃,沸点–10℃;SO3熔点16.8℃,沸点44.8℃。
(1)实验③反应的离子方程式是 。
(2)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有______气体,依据是 。
(3)实验④反应的离子方程式是__ _____。
(4)某同学依据B中的现象,认为FeSO4分解一定有SO3生成。你认为是否正确,原因是(用必要的文字和化学方程式解释)___ __ (填“正确”或“不正确”)理由
。
查看答案和解析>>
科目:高中化学 来源: 题型:
 而与具体反应进行的途径无关。物质A在一定条件下可发生一系列转化,由右图判断下列
而与具体反应进行的途径无关。物质A在一定条件下可发生一系列转化,由右图判断下列
关系错误的是
A.A→F,△H = - △H 6
B.△H1+△H 2+△H 3+△H 4+△H 5+△H 6=1
C.C→F,|△H| = |△H 1+△H 2+△H 6 |
D.△H 1+△H 2+△H 3 = -△H 4-△H5-△H 6
查看答案和解析>>
科目:高中化学 来源: 题型:
碘与氢气反应的热化学方程式为:
①I2(g)+H2(g) 2HI(g) ΔH= - 9.48 kJ·mol-1
2HI(g) ΔH= - 9.48 kJ·mol-1
②I2(s)+H2(g) 2HI(g) ΔH= + 26.48 kJ·mol-1,由此判断下列说法或反应正确的是
2HI(g) ΔH= + 26.48 kJ·mol-1,由此判断下列说法或反应正确的是
A.反应①的产物比反应②的产物稳定
B.I2(s) I2(g) ΔH= + 17.00 kJ·mol-1
I2(g) ΔH= + 17.00 kJ·mol-1
C.反应②的反应物总能量比反应①的反应物总能量低
D.1 mol I2(g)中通入1 mol H2(g),反应后放热9.48 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作正确的是
A.过滤时为加快速度,可先将上层清液注入过滤器中,再将沉淀转移到过滤器中
B.蒸发时用玻璃棒搅拌,是为了使析出的固体重新溶解
C.蒸馏时需从冷凝管上口进水,下口出水
D.分液时,下层液体放完后,再从下口放出上层液体
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中发生如下反应:aX(g)+bY(g) cZ(g)+dW(g),反应达平衡后,W的浓度为0.5mol•L-1,保持温度不变,将气体压缩到原来的一半体积,当再次达到平衡时,W的浓度为0.8mol•L-1。下列叙述不正确的是 ( )
A.平衡向逆反应方向移动 B.a+b > c+d
C.Z的体积分数减少 D.X的转化率减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com