
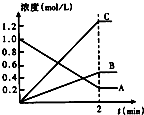
| 0.8mol/L |
| 2min |
| C2(C) |
| C(A).C3(B) |
| C2(C) |
| C(A).C3(B) |


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源:不详 题型:单选题
| A.容器中的总压强不随时间的变化而变化 |
| B.单位时间内有nmolA2生成同时就有nmolB2生成 |
| C.单位时间内有nmolA2生成同时就有2nmolAB生成 |
| D.单位时间内有nmolB2生成同时就有2nmolAB分解 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
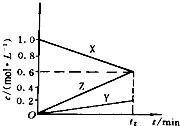
科目:高中化学 来源:不详 题型:单选题
| A.正反应为吸热反应,C是固体或液体 |
| B.正反应为吸热反应,C是气体 |
| C.正反应为放热反应,C是气体 |
| D.正反应为放热反应,C是固体或液体 |

查看答案和解析>>
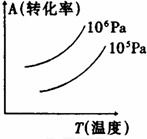
科目:高中化学 来源:不详 题型:单选题
| A.正反应是吸热反应 |
| B.(m+n)<(p+q) |
| C.压强增大,A的转化率减小 |
| D.温度升高,A的转化率减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| c(H2)?c(CO) |
| c(H2O) |
| n(CH4) |
| n(H2O) |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com