
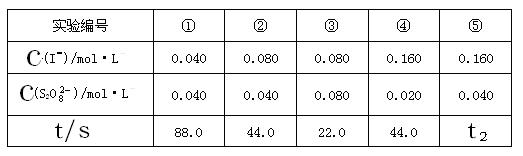
| A.<22.0s | B.22.0~44.0s | C.>44.0s | D.数据不足,无法判断 |


科目:高中化学 来源:不详 题型:填空题
| 实验编号 | T/K | 大理石规格 | HNO3浓度/mol·L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和__探究温度对该反应速率的影响; (Ⅲ)实验①和__探究大理石规格(粗、细)对该反应速率的影响。 |
| ② | | | | |
| ③ | | 粗颗粒 | | |
| ④ | | | |
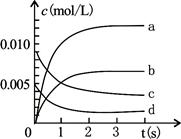
 2NO2(g),正反应放热。测得n(NO)随时间的变化如下表,请回答:
2NO2(g),正反应放热。测得n(NO)随时间的变化如下表,请回答:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2CO(g)反应中可使反应速率增大的措施是 ( )
2CO(g)反应中可使反应速率增大的措施是 ( )| A.①③⑤ | B.②④⑥ | C.①③⑥ | D.③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③⑦ | B.②④⑥ | C.②③⑥ | D.①⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaNO3 溶液 | B.CuSO4或石墨 | C.Na2SO4溶液 | D.NaHSO3 或CuO |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na2SO4(s) | B.NaOH | C.(NH4)2SO4(s)? | D.CH3COONa溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.增大反应物浓度,可增大活化分子的百分数,从而使有效碰撞次数增多 |
| B.有气体参加的反应,若增大压强,可增大活化分子的百分数,从而使反应速率增大 |
| C.升高温度能使反应速率增大的主要原因是减小了反应物分子中活化分子的百分数 |
| D.催化剂能增大单位体积内活化分子的百分数,从而成千上万倍地增大反应速率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 组别 | 10%硫酸的体积(mL) | 温度/℃ | 其他物质 |
| ① | 2 mL | 20 | |
| ② | 2 mL | 20 | 10滴饱和MnSO4溶液 |
| ③ | 2 mL | 30 | |
| ④ | 1 mL | 20 | 1 mL蒸馏水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com