
����Ŀ��̼�����׳ƴ�����ճ���������������Ź㷺��Ӧ�ã�ij��ѧ��ȤС���������ѧ֪ʶģ���Ʊ�̼���ƣ��������£�����NaCl��NH3��CO2��ˮ��Ϊԭ���Լ���ͼ��ʾװ����ȡNaHCO3����Ӧ�Ļ�ѧ����ʽΪNH3 + CO2 + H2O + NaCl = NaHCO3��+ NH4Cl����Ȼ���ٽ�NaHCO3�Ƴ�Na2CO3��
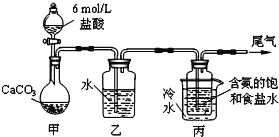
��1��װ���ҵ�������_________��Ϊ��ֹ��Ⱦ������β���к��е�_________��Ҫ�������մ�����
��2����װ�ñ��в�����NaHCO3��ȡNa2CO3ʱ����Ҫ���е�ʵ�������______��_______��____��NaHCO3ת��ΪNa2CO3�Ļ�ѧ����ʽΪ_____________��
��3�����ڣ�2���з�Ӧʱ��϶̣�NaHCO3���ֽⲻ��ȫ����С���һ�ݼ�����t1 min��NaHCO3��Ʒ����ɽ���������̽����ȡ������t1 min��NaHCO3��Ʒ27.4g��ȫ����ˮ�Ƴ���Һ��Ȼ�������Һ�в��ϵμ�1mol��L��1��ϡ����ֱ�����ٲ������ݣ�������400 mLϡ���ᡣ��ش��������⣺
������ʵ�����Ҫ�����ܶ�Ϊ1.19g ��cm��3 ��������Ϊ36.5%��Ũ��������1mol��L��1��ϡ����ʱ����Ҫ�õ��IJ����������ձ�������������Ͳ����ͷ�ιܺ�____�����������ƣ�����Ҫ��ȡ��Ũ�������Ϊ��_____mL��
�� ����Ʒ��NaHCO3��Na2CO3�����ʵ���֮����_____��
���𰸡���ȥ������̼�е��Ȼ������� ���� ���� ϴ�� ���� 2NaHCO3 ![]() Na2CO3 + H2O + CO2�� 500mL����ƿ 42 2��1
Na2CO3 + H2O + CO2�� 500mL����ƿ 42 2��1
��������
ʵ���У�ϡ�����̼��Ʒ�Ӧ���ɶ�����̼����Ӧ����ʽΪCaCO3+2HCl=CaCl2+H2O+CO2����������лӷ��ԣ��������ɵĶ�����̼�к���HCl��HCl��������ˮ��������ˮϴ�������ϴ����Ķ�����̼ͨ�뺬���ı���ʳ��ˮ�У������ķ�ӦΪNH3+CO2+H2O+NaCl=NaHCO3��+NH4Cl��β���к��а������Ի���������Ⱦ������β��Ҫ���д������ݴ˷������
(1)HCl��������ˮ����ϡ���ᣬ̼������С�����ᣬ��Ȼ������̼������ˮ������������ϡ�����У������д̼�����ζ����Ⱦ������β���к��а���������β��Ҫ���д������ʴ�Ϊ����ȥ������̼�е��Ȼ������壻������
(2)���õ���̼�����ƹ��ˡ�ϴ�ӵõ��ϸɾ���̼�����ƣ�̼�����Ʋ��ȶ�������̼�����Ƶõ�̼���ƣ���Ӧ����ʽΪ2NaHCO3 ![]() Na2CO3+H2O+CO2�����ʴ�Ϊ�����ˣ�ϴ�ӣ����գ�2NaHCO3
Na2CO3+H2O+CO2�����ʴ�Ϊ�����ˣ�ϴ�ӣ����գ�2NaHCO3 ![]() Na2CO3+H2O+CO2����
Na2CO3+H2O+CO2����
(3)��ʵ����û��400mL����ƿ����Ӧ��ѡȡ500mL����ƿ���ƣ��ܶ�Ϊ1.19g ��cm��3 ��������Ϊ36.5%��Ũ��������ʵ���Ũ��c=![]() =
=![]() mol/L =11.9mol/L����Һϡ��ǰ�����ʵ����ʵ������䣬��Ũ�������=
mol/L =11.9mol/L����Һϡ��ǰ�����ʵ����ʵ������䣬��Ũ�������=![]() =42mL���ʴ�Ϊ��500mL����ƿ��42��
=42mL���ʴ�Ϊ��500mL����ƿ��42��
��400 mL1mol��L��1��ϡ�����к���0.4molHCl����NaHCO3��Na2CO3�����ʵ����ֱ���xmol��ymol��̼�����ơ�̼���Ʒֱ���Ҫ�������ʵ���Ϊxmol��2ymol���У�84x+106y��27.4��x+2y��0.4����ã�x��0.2��y��0.1����NaHCO3��Na2CO3�����ʵ���֮��=0.2mol��0.1mol=2��1���ʴ�Ϊ��2��1��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼��ͭ�������仯������������;���ش���������
��1����Ԫ�����ڱ���������̼ͬ�������ڵ������ڡ���̬��ԭ�ӵļ۵����Ų�ʽΪ__________���ݴ��Ʋ������ij���������__________��
��2����ͭ(Cu3P2)������������ͭ������ͭ�Ǻ�����������ͭ�Ͻ���ͭ��ˮ��Ӧ�����ж�������(PH3)������PH3���ӵĿռ乹��Ϊ__________��P��S�ĵ�һ������(I1)�Ĵ�СΪI1(P) __________I1(S)(�>����<����=��)
��3��CO32����Cԭ�ӵ��ӻ��������Ϊ__________����ϩ������������м���Ŀ֮��Ϊ__________��
��4��NH3�ķе�__________(����ڡ����ڡ�)PH3�ķе���ԭ����____________________��
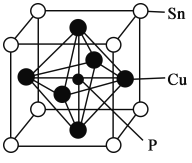
��5������ͭ����ľ����ṹ��ͼ��ʾ���þ�����Pԭ��λ����ͭԭ���γɵ�__________�Ŀ�϶�С��������ܶ�Ϊag��cm��3��P�������Cuԭ�ӵĺ˼��Ϊ__________nm(�ú�NA�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������У����������Ȳ���������Ȼ��������ܽ⡱������ǣ� ��
A. ��ϡ��������μ��������![]() ��Һ
��Һ
B. ��![]() ��Һ����μ������ϡ
��Һ����μ������ϡ![]() ��Һ
��Һ
C. ��![]() ��Һ����μ���ϡ��ˮ
��Һ����μ���ϡ��ˮ
D. ������������Һ��ͨ�����![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ƿ���Ϊ���ȼ�����֪25.0 mL 0.100 mol��L��1 Na2S2O3��Һǡ�ð�112 mL Cl2����״���£���ȫת��ΪCl�����ӣ���S2O32����ת����
A.SO42��B.SO32��C.SD.S2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȫ��̬����������ܶȸߡ��ɱ��ͣ��乤��ԭ����ͼ��ʾ�����е缫 a���ò���ʯīϩ��S8���ϣ���ط�ӦΪ��16Li+xS8=8Li2Sx��2��x��8��������˵��������ǣ� ��

A. ��ع���ʱ�������ɷ�����Ӧ��2Li2S6+2Li++2e-=3Li2S4
B. ��ع���ʱ�����·������ 0.02 mol ���ӣ��������ϼ��� 0.14 g
C. ʯīϩ��������Ҫ����ߵ缫a�ĵ�����
D. ��س��ʱ��Խ���������Li2S2����Խ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ӵ�������ֵΪ![]() ������˵����ȷ����
������˵����ȷ����
A. 1L0.1mol��![]() NH4Cl��Һ�У�
NH4Cl��Һ�У� ![]() ������Ϊ0.1
������Ϊ0.1![]()
B. 2.4gMg��H2SO4��ȫ��Ӧ��ת�Ƶĵ�����Ϊ0.1![]()
C. ��״���£�2.24LN2��O2�Ļ�������з�����Ϊ0.2![]()
D. 0.1mol H2��0.1mol I2���ܱ������г�ַ�Ӧ�����������Ϊ0.2![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���̷��Ǻ���һ�����ᾧˮ�������������ڹ�ũҵ�����о�����Ҫ����;��ij��ѧ��ȤС����̷���һЩ���ʽ���̽�����ش��������⣺
��1�����Թ��м��������̷���Ʒ����ˮ�ܽ⣬�μ�KSCN��Һ����Һ��ɫ�����Ա仯�������Թ���ͨ���������Һ��졣�ɴ˿�֪��______________��_______________��
��2��Ϊ�ⶨ�̷��нᾧˮ��������ʯӢ�����ܣ����˿���K1��K2������Ϊװ��A�����أ���Ϊm1 g������Ʒװ��ʯӢ�������У��ٴν�װ��A���أ���Ϊ m2 g������ͼ���Ӻ�װ�ý���ʵ�顣

������B��������____________________��
�ڽ�����ʵ�����������ȷ����___________________�����ţ����ظ������������裬ֱ��A���أ���Ϊm3 g��
a.��ȼ�ƾ��ƣ����� b.Ϩ��ƾ��� c.�ر�K1��K2
d.��K1��K2������ͨ��N2 e.����A f.��ȴ������
�۸���ʵ���¼�������̷���ѧʽ�нᾧˮ��Ŀx=________________����ʽ��ʾ������ʵ��ʱ��a��d�����������ʹx__________���ƫ��ƫС������Ӱ�족����
��3��Ϊ̽�����������ķֽ�������2�����Ѻ��ص�װ��A������ͼ��ʾ��װ���У���K1��K2������ͨ��N2�����ȡ�ʵ���Ӧ���в�������Ϊ��ɫ��ĩ��

��C��D�е���Һ����Ϊ_________�����ţ���C��D��������ð�������ɹ۲쵽������ֱ�Ϊ_______________��
a��Ʒ�� b��NaOH c��BaCl2 d��Ba(NO3)2 e��ŨH2SO4
��д�������������·ֽⷴӦ�Ļ�ѧ����ʽ_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵�����ʾ������ȷ�ģ�������
A. ��ϡ��Һ�У�![]() ��
��![]() ��������
��������![]() �������뺬1molNaOH����Һ��ϣ��ų�����һ��Ϊ
�������뺬1molNaOH����Һ��ϣ��ų�����һ��Ϊ![]()
B. ��![]() ʯī
ʯī![]() ���ʯ
���ʯ![]() ��
��![]() ��֪�����ʯ��ʯī�ȶ�
��֪�����ʯ��ʯī�ȶ�
C. ʵ���û�����![]() ������ϩ
������ϩ![]() �ͱ�
�ͱ�![]() �ı�ȼ�շֱ�Ϊ
�ı�ȼ�շֱ�Ϊ![]() ��
��![]() ��
��![]() ������֤���ڱ������в����ڶ�����̼̼˫��
������֤���ڱ������в����ڶ�����̼̼˫��
D. ��101kPaʱ��![]() ��ȫȼ������Һ̬ˮ���ų�
��ȫȼ������Һ̬ˮ���ų�![]() ���������ʾ����ȼ���ȵ��Ȼ�ѧ����ʽΪ��
���������ʾ����ȼ���ȵ��Ȼ�ѧ����ʽΪ��![]() ��
��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(Na3AlF6)�ǹ�ҵ��������Ҫ�ĺ������Ӽ���ʵ�����Է�ʯ(CaF2)��ʯӢ�ʹ���Ϊԭ��ģ�ҵ�Ʊ��������Ƶ��������£�
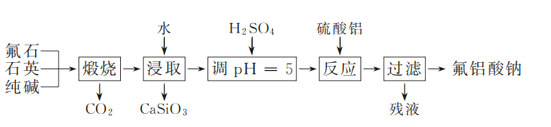
(1) �����ա�ʱ������ҩƷ��Ϻ�Ӧ����________(����������)�м��ȡ�
(2) ͨ�����Ʒ�Һ©���Ļ������Ե�������Һ������ʡ�����ҺpH�ӽ�5ʱ���μ�ϡ����ķ�Һ©���Ļ���Ӧ����ͼ�е�________(�����)��ʾ��

(3) �����Է�ˮ�м���Al2(SO4)3��Na2SO4�����Һ���ɽ���ˮ��F��ת��Ϊ�������Ƴ�����
�� �û����Һ�У�Al2(SO4)3��Na2SO4�����ʵ���֮��Ӧ��________(����ֵ)��
���ڲ��ı���������������£�����NaOH������ҺpH��ʵ������Һ�в�����Ũ�Ⱥͷ�ȥ��������ҺpH�ı仯��ϵ��ͼ��ʾ��pH>5ʱ����Һ�в�����Ũ�������ԭ����________��
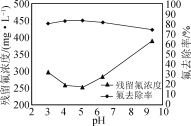
(4) ����CaCl2��Ϊ��������ȥF������ʹF��Ũ�Ȳ�����0.95 mg��L��1��c(Ca2��)����Ϊ________mol��L��1��[Ksp(CaF2)��2.7��10��11]
(5) ��ҵ����м(��Ҫ�ɷ�Ϊ����������������������)��������ȡ����������[Al2(SO4)3��18H2O]��
���벹�������ɷ���мΪԭ���Ʊ������������ʵ�鷽����ȡһ��������м�������ձ��У�____________________________________________________________�������������塣[��֪��pH��5ʱ��Al(OH)3������ȫ��pH��8.5ʱ��Al(OH)3������ʼ�ܽ⡣��ʹ�õ��Լ���3 mol��L��1 H2SO4��Һ��2 mol��L��1 NaOH��Һ����ˮ]
��ʵ����������У�Ӧ����ǿ��ͨ�磬ԭ����________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com