
| A、氮气是还原产物,二氧化碳是氧化产物 |
| B、HNCO中碳元素被氧化 |
| C、1molHNCO参加反应失去3mol电子 |
| D、氧化产物与还原产物质量比为1:1 |


科目:高中化学 来源: 题型:
| A、HIO与HCN均为含有极性键的直线形极性分子 |
| B、SiO2与C02均为每摩含有4×6.02×1023对共用电子对的酸性氧化物 |
| C、Na2S浓溶液与稀盐酸分别滴加到饱和AgCl溶液中均一定有沉淀产生 |
| D、明矾与离子交换树脂均能将海水进行淡化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸 | HCOOH | HNO2 | H2S | H2SO3 | H2C2O4 |
| 电离平衡常数(25℃) | K=1.8×10-4 | K=5.1×10-4 | K1=9.1×10-8 K2=1.1×10-12 | K1=1.23×10-2 K2=6.6×10-8 | K1=5.4×10-2 K2=5.4×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
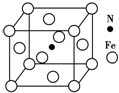 铁及其化合物在有机化学中应用广泛,例如有机合成中,常用铁和盐酸将硝基(-NO2)还原为氨基(-NH2);在苯的溴代反应中用溴化铁作催化剂.
铁及其化合物在有机化学中应用广泛,例如有机合成中,常用铁和盐酸将硝基(-NO2)还原为氨基(-NH2);在苯的溴代反应中用溴化铁作催化剂.查看答案和解析>>
科目:高中化学 来源: 题型:

| A、离子半径的大小顺序为W>Q>Y>Z |
| B、X、Y、W三种元素的电负性大小顺序为X>Y>W |
| C、X、Z、W三种元素的最高价氧化物对应的水化物均能与强碱反应 |
| D、元素X的最简单氢化物与Q的氢化物化合的产物中既含共价键又含离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,分子数为NA的N2、C2H4混合气体的总质量为28g |
| B、0.1mol Mg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数目为0.2NA |
| C、60gCaCO3与KHCO3的混合物与足量盐酸反应生成CO2分子数为0.6NA |
| D、常温常压下,将0.1mol氯气通入水中发生化学反应,转移电子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、胆矾、漂白粉、氯化钾、氯气 |
| B、冰醋酸、福尔马林、硫酸钠、乙醇 |
| C、单甘油酯、混甘油酯、苛性钾、石灰石 |
| D、盐酸、水煤气、醋酸、干冰 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com