
【题目】一定条件下,在体积为3L的密闭容器中化学反应CO(g)+2H2(g)![]() CH3OH(g)达到平衡状态.判断可逆反应达到平衡状态的标志是( )
CH3OH(g)达到平衡状态.判断可逆反应达到平衡状态的标志是( )
A.υ生成(CH3OH)=υ消耗(CO)B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变D.CO、H2、CH3OH的浓度相等
【答案】C
【解析】
可逆反应CO(g)+2H2(g)![]() CH3OH(g)为气体体积缩小的反应,当正逆反应速率相等时,各组成成分的浓度、百分比含量等不在变化,说明达到平衡状态,据此回答。
CH3OH(g)为气体体积缩小的反应,当正逆反应速率相等时,各组成成分的浓度、百分比含量等不在变化,说明达到平衡状态,据此回答。
A. υ生成(CH3OH)=υ消耗(CO),表示的都是正反应速率,无法判断正逆反应速率是否相等,则无法判断是否达到平衡状态,故A错误;
B.该反应前后都是气体,气体总质量不变,容器为恒容容器,体积不变,则气体密度不会发生改变,则无法判断是否达到平衡状态,故B错误;
C.该反应为气体体积缩小的反应,气体的物质的量发生变化,而气体总质量不变,则混合气体的平均相对分子质量为变量,当混合气体的平均相对分子质量不再改变时达到平衡状态,故C正确;
D. CO、H2、CH3OH的浓度相等无法判断各组分的浓度是否变化,无法判断是否达到平衡状态,故D错误;
故答案选:C。


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案科目:高中化学 来源: 题型:
【题目】已知某种燃料含有碳、氢、氧三种元素。为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的O2中燃烧,并使产生的气体全部通过如图所示装置中,得到如表中所列的实验结果(假设产生的气体完全被吸收)。
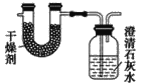
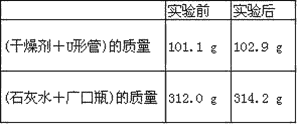
根据实验数据求:
(1)实验完毕后,生成物中水的质量为________g。假设广口瓶里生成一种正盐,其质量为_____________g。
(2)生成的水中氢元素的质量为_______g。
(3)生成的二氧化碳中碳元素的质量为_______ g。
(4)该燃料中碳元素与氢元素的质量比为_______。
(5)已知这种燃料的每个分子中含有一个氧原子,则该燃料的分子式为_______,结构简式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,则下列说法正确的是
A. 0.4mol AgNO3受热完全分解(2AgNO3![]() 2Ag+2NO2↑+O2↑),用排水法最终收集到气体的分子数为0.2NA
2Ag+2NO2↑+O2↑),用排水法最终收集到气体的分子数为0.2NA
B. 6.4g CaC2中含有的离子总数目为0.3NA
C. 1 mol FeI2与一定量氯气反应时,若已知有1mol Fe2+被氧化则转移的电子数为3NA
D. 1mol 苯和苯甲酸的混合物完全燃烧时消耗O2的分子数为7.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从古至今,铁及其化合物在人类生产生活中的作用发生了巨大变化。
(1)古代中国四大发明之一的指南针是由天然磁石制成的,其主要成分是______(填字母序号)。
a.Fe b.FeO c.Fe3O4 d.Fe2O3
(2)硫酸渣的主要化学成分为:SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):
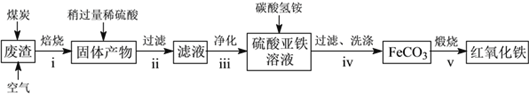
回答下列问题:
①在步骤i中产生的有毒气体可能有__________________。
②在步骤iii操作中,要除去的离子之一为Al3+。若常温时Ksp[Al(OH)3]=1.0×10-32,此时理论上将Al3+沉淀完全,则溶液的pH为____________。
③步骤iv中,生成FeCO3的离子方程式是_________________。
(3)氯化铁溶液称为化学试剂中的“多面手”,向氯化铜和氯化铁的混合溶液中加入氧化铜粉末会产生新的沉淀,写出该沉淀的化学式_________________。请用平衡移动的原理,结合必要的离子方程式,对此现象作出解释:___________________。
(4)①古老而神奇的蓝色染料普鲁士蓝的合成方法如下:

复分解反应ii的离子方程式是________________。
②如今基于普鲁士蓝合成原理可检测食品中CN-,方案如下:
![]()
若试纸变蓝则证明食品中含有CN-,请解释检测时试纸中FeSO4的作用:
_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是
A.  Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
B.  正极的电极反应式为Ag2O+2e+H2O2Ag+2OH
正极的电极反应式为Ag2O+2e+H2O2Ag+2OH
C.  锌筒作负极,发生氧化反应,锌筒会变薄
锌筒作负极,发生氧化反应,锌筒会变薄
D.  使用一段时间后,电解质溶液的酸性减弱,导电能力下降
使用一段时间后,电解质溶液的酸性减弱,导电能力下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应X(g)+Y(g) ![]() nZ(g) ΔH >0,将X和Y以一定比例混合通入密闭容器中进行反应,各物质的浓度随时间的改变如图所示。下列说法不正确的是( )
nZ(g) ΔH >0,将X和Y以一定比例混合通入密闭容器中进行反应,各物质的浓度随时间的改变如图所示。下列说法不正确的是( )
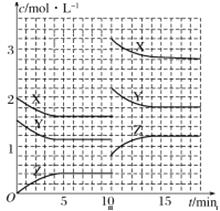
A.反应方程式中n=1
B.10min时,曲线发生变化的原因是升高温度
C.10min时,曲线发生变化的原因是增大压强
D.前5min后,用X表示的反应速率为v(X)=0.08mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() +CH2=CH-M
+CH2=CH-M![]() +HX(X为卤原子,M为烃基或含酯基的取代基等).由有机物A合成G(香豆素)的路线如下:
+HX(X为卤原子,M为烃基或含酯基的取代基等).由有机物A合成G(香豆素)的路线如下:

(1)写出C中的含氧官能团的名称__,F→G的反应类型是__;
(2)写出A与银氨溶液反应的化学方程式:_______;
(3)D的结构简式为__;
(4)F有多种同分异构体,写出同时满足下列条件的F的一种同分异构体的结构简式:_____;
Ⅰ.分子中除苯环外,无其他环状结构;
Ⅱ.苯环上有两个处于对位的取代基;
Ⅲ..能发生水解反应,不能与金属Na反应;
Ⅳ.能与新制的Cu(OH)2按物质的量之比1:2发生反应;
(5)二氢香豆素(![]() )常用作香豆素的替代品.鉴别二氢香豆素和它的一种同分异构体(
)常用作香豆素的替代品.鉴别二氢香豆素和它的一种同分异构体(![]() )需要用到的试剂有:NaOH溶液________、________;
)需要用到的试剂有:NaOH溶液________、________;
(6)已知:![]() R、R′为烃基),请写出以苯、丙烯(CH2═CHCH3)为原料制备
R、R′为烃基),请写出以苯、丙烯(CH2═CHCH3)为原料制备![]() 的合成路线流程图____________(无机试剂任选).合成路线流程图示例如下:H2C═CH2
的合成路线流程图____________(无机试剂任选).合成路线流程图示例如下:H2C═CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH。
CH3CH2OH。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2﹣羟基异丁酸乙酯能溶于水,是一种应用于有机合成和药物制造的化工原料。

(1)2﹣羟基异丁酸乙酯的分子式为_________,不同化学环境的氢在核磁共振氢谱图中有不同的吸收峰,则2﹣羟基异丁酸乙酯有_________个吸收峰;
(2)①②的反应类型分别为_________,_________;
(3)已知I为溴代烃,I→B的化学方程式为_________;
(4)缩聚产物F的结构简式为_________;
(5)下列关于![]() 和
和 的说法正确的有_________(双选,填字母);
的说法正确的有_________(双选,填字母);
A.后者遇到FeCl3溶液显紫色,而前者不可
B.两者都可以与NaHCO3溶液反应放出CO2
C.两者都可以与氢氧化钠溶液发生反应,当两者物质的量相等时,消耗氢氧化钠的量不相等
D.两者都可以与氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡鞣酸具有较广泛的抗菌作用,其结构简式如下图所示:

关于咖啡鞣酸的下列叙述正确的是( )
A.分子式为C16H13O9
B.1 mol咖啡鞣酸可与含8 mol NaOH的溶液反应
C.能使酸性KMnO4溶液褪色,说明分子结构中含有碳碳双键
D.与浓溴水能发生两种类型的反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com