
某校兴趣小组用如图Ⅰ装置制取漂白液(气密性已检验,试剂已添加),并研究其相关性质。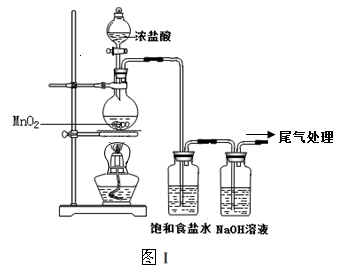

实验操作和现象:打开分液漏斗的活塞,缓缓滴加一定量浓盐酸,点燃酒精灯;一段时间后,关闭分液漏斗的活塞,熄灭酒精灯。
(1)烧瓶中反应的化学方程式是 。
(2)饱和食盐水的作用是 。
(3)若用图Ⅱ装置收集多余的氯气,请在虚线框内画出该装置简图。
(4)该小组同学用上述装置制得的漂白液中NaClO的浓度偏低。
查阅资料:在溶液中发生反应:
(a)Cl2(g)+2NaOH(aq)═ NaCl(aq)+NaClO(aq)+H2O(l)??H1=-101.1kJ/mol
(b)3NaClO(aq)═2NaCl(aq)+NaClO3(aq)??H2=-112.2kJ/mol
反应(a)的反应速率很快,反应(b)在室温下较慢
根据资料,请对图Ⅰ装置提出改进建议: 。
(5)修改方案后,该小组同学制得了较高浓度的NaClO溶液。他们把漂白液和滴有酚酞的红色Na2SO3溶液混合后,得到无色溶液。
提出猜想:ⅰ.NaClO把Na2SO3氧化了
ⅱ.NaClO把酚酞氧化了
ⅲ.NaClO把Na2SO3和酚酞均氧化了
①下列实验方案中可以证明NaClO氧化了Na2SO3的是 。
a.向混合后的溶液中加入过量盐酸
b.向混合后的溶液中加入过量盐酸,再加入氯化钡溶液
c.向混合后的溶液中加入过量硝酸,再加入硝酸银溶液
d.向混合后的溶液中加入氢氧化钡溶液,再加入过量盐酸
②为证明NaClO氧化了酚酞,可进行的实验是 。
(1)MnO2+4HCl(浓) 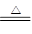 MnCl2+Cl2↑+2H2O(2)除去氯气中的氯化氢
MnCl2+Cl2↑+2H2O(2)除去氯气中的氯化氢
(3) (4)将盛NaOH溶液的洗气瓶浸在冰水中 (5)①b d ②向混合后的溶液中加入NaOH溶液,若溶液不变红说明酚酞已经被氧化;若溶液变红说明酚酞没有被氧化。
(4)将盛NaOH溶液的洗气瓶浸在冰水中 (5)①b d ②向混合后的溶液中加入NaOH溶液,若溶液不变红说明酚酞已经被氧化;若溶液变红说明酚酞没有被氧化。
解析试题分析:(1)烧瓶中反应的化学方程式是MnO2+4HCl(浓) 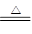 MnCl2+Cl2↑+2H2O,注意:①要写有加热符号;②必须为浓盐酸。(2)饱和食盐水的作用是除去氯气中混有的氯化氢气体;饱和氯化钠溶液可以降低氯气的溶解度;饱和氯化钠溶液可吸收氯化氢气体。(4)温度降低可以促进次氯酸钠的生成,所以我们可以将装置浸泡在冰水里。(5)只要能检验出硫酸根离子的存在,就可以证明NaClO氧化了Na2SO3。检验硫酸根离子办法:向混合后的溶液中加入过量盐酸,再加入氯化钡溶液,如果产生白色沉淀就能证明硫酸根离子的存在;向混合后的溶液中加入氢氧化钡溶液,再加入过量盐酸,如果还能生成白色沉淀就证明硫酸根离子的存在。②为证明NaClO氧化了酚酞,只要向混合后的溶液中加入NaOH溶液,若溶液不变红说明酚酞已经被氧化;若溶液变红说明酚酞没有被氧化。
MnCl2+Cl2↑+2H2O,注意:①要写有加热符号;②必须为浓盐酸。(2)饱和食盐水的作用是除去氯气中混有的氯化氢气体;饱和氯化钠溶液可以降低氯气的溶解度;饱和氯化钠溶液可吸收氯化氢气体。(4)温度降低可以促进次氯酸钠的生成,所以我们可以将装置浸泡在冰水里。(5)只要能检验出硫酸根离子的存在,就可以证明NaClO氧化了Na2SO3。检验硫酸根离子办法:向混合后的溶液中加入过量盐酸,再加入氯化钡溶液,如果产生白色沉淀就能证明硫酸根离子的存在;向混合后的溶液中加入氢氧化钡溶液,再加入过量盐酸,如果还能生成白色沉淀就证明硫酸根离子的存在。②为证明NaClO氧化了酚酞,只要向混合后的溶液中加入NaOH溶液,若溶液不变红说明酚酞已经被氧化;若溶液变红说明酚酞没有被氧化。
考点:考查氯气的制备和氯气相关的化学性质。


科目:高中化学 来源: 题型:实验题
某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验,请回答下列问题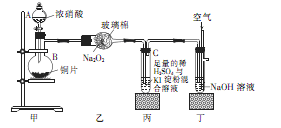
(1)装置甲中盛放浓硝酸的仪器A的名称是 ,仪器B中发生反应的化学方程式为
(2)完成下面表格中的空白
(3)取下装置丙中的试管C,向其中滴加足量的Na2SO3溶液,溶液颜色褪去,该过程中发生反应的离子方程式为 。反应后的溶液中主要含有SO32—、SO42—、I—等阴离子,请填写鉴定SO32—、SO42—和I—的实验报告。
限选试剂:2mol·L—1HCl、1mol·L—1H2SO4、1mol·L—1BaCl2、1mol·L—1Ba(NO3)2、CCl4、新制饱和溴水、新制饱和氯水。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某化学兴趣小组利用图一装置制取氨气并探究氨气的有关性质。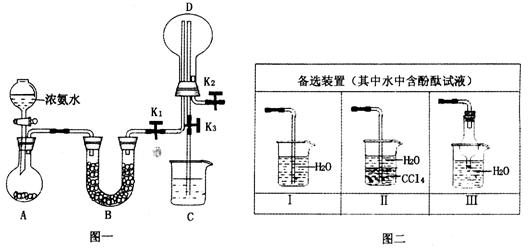
(1)装置A中烧瓶内试剂可选用________(填序号)
a.碱石灰 b.浓硫酸 c.生石灰 d.五氧化二磷 e.烧碱
(2)若探究氨气的溶解性,需在K2的导管末端连接图二装置中的_____装置(填序号),当装置D中集满氨气后,关闭K1、K2,打开K3,引发喷泉的实验操作是______________
___________________________________________________________________________。
(3)若探究氨气的还原性,需打开K1、K2,K3处导管连接制取纯净、干燥氯气的装置。
①用二氧化锰与浓盐酸制取氯气,生成气体必须通过盛有____________试剂的洗气瓶;
②D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为___________________________________;
③从K3处导管逸出的气体中含有少量Cl2,则C装置中应盛放_________溶液(填化学式),反应的离子方程式为____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(1)向蓝色石蕊试纸上滴加几滴饱和氯水,发现试纸先变红后变白。要确证使石蕊褪色的物质是次氯酸,还必须要做的实验是 :
a.干燥的氯气能否使试纸变白 b.水能否使试纸变白 c.盐酸能否使试纸变白
(2)饱和氯水与石灰石的反应是制取较浓HC1O溶液的方法之一。如图所示在试管中加入过量的块状碳酸钙.再加入约20ml饱和氯水充分反应,有少量气泡产生,溶液浅黄绿色褪去:过滤,将滤 液滴在蓝色石蕊试纸上发现其漂白性比饱和氯水的更强:已知饱和氨水中存在Cl2+H2O H++C1-+HClO.反应后所得的溶液漂白性增强的原因是 (用化学平衡移动原理解释)。
H++C1-+HClO.反应后所得的溶液漂白性增强的原因是 (用化学平衡移动原理解释)。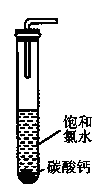
(3)碳酸钙与氯水反应生成的含钙的化合物除氯化钙外,有人提出如下猜想
a.含次氯酸钙 b.含碳酸氢钙 c.含次氯酸钙和碳酸氢钙。
有人认为不可能含有次氯酸钙.他的理由可能是 。
为了证明碳酸氢钙的存在,将滤液分为三份.分别进行以下实验:
①第一份与澄清石灰水混合,立即产生大量白色沉淀:此实验____(填“能”或“不能”)确证溶液中含有碳酸氢钙因为 ;
②第二份与稀盐酸混合,立即产生大量无色气体:
③将第三份加热,看到溶液变浑浊且有大量无色气体产生。反应的化学方程式为
④除上述实验外,你能设计的确证碳酸氢钙存在的实验方案是____。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某研究小组探究:
I .铜片和浓硫酸的反应(夹持装置和A中加热装置已略,气密性已检验)
II. SO2和 Fe( NO3)3溶液的反应[1.0 mol/L的 Fe(NO3)3溶液的 pH=1]请回答下列有关问题:
探究I
(l)某学进行了下列实验:取12.8g铜片和20 mL 18 mol?L-1的浓硫酸放在三颈瓶中共热,直至反应完毕,最后发现烧瓶中还有铜片剩余,同时根据所学的知识同学们认为还有较多的硫酸剩余。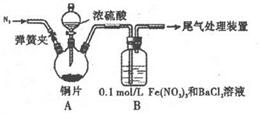
①装置A中反应的化学方程式是_______
②该同学设计求余酸浓度的实验方案是测定产生气体的量。其方法有多种,请问下列方案中不可行的是______ (填字母)。
| A.将产生的气体缓缓通过预先称量的盛有碱石灰的干燥管,结束反应后再次称貴 |
| B.将产生的气体缓缓通入酸性髙锰酸钾溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀 |
| C.用排水法测定其产生气体的体积(折算成标准状况) |
| D.用排饱和NaHSO3溶液的方法测定其产生气体的体积(折算成标准状况) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
硫酸是工业生产中重要的产品之一,以黄铁矿为原料生产硫酸的简单流程如下图所示。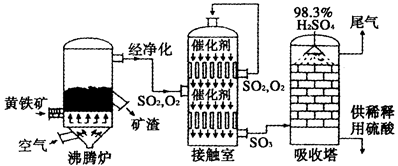
请填写下列空白。
(1)黄铁矿燃烧生成SO2的化学方程式为_____________;接触室中发生反应的化学方程式为____________________。
(2)为充分利用反应放出的热量,接触室中应安装_____________(填设备名称);吸收塔中填充有许多瓷管,其作用为__________________。
(3)为使黄铁矿煅烧充分,常通入过量40%的空气,则煅烧后炉气中SO2的体积分数为____________________(设空气中氧气的体积分数为0.20);将上述炉气经净化除尘后直接送入接触室,流量为1.00m3/s,从接触室导出气体的流量为0.95m3/s(同温同压下测定),则SO2的转化率为________________%。
(4)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐。SO2既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2。SO2吸收Br2的离子方程式为___________________。
(5)硫酸的用途非常广泛,可应用于下列____________(可多选)。
a.橡胶的硫化 b.过磷酸钙的制备
c.铅蓄电池的生产 d.表面活性剂“烷基苯磺酸钠”的合成
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物。下表各组物质之间通过一步反应不能实现如图所示转化的是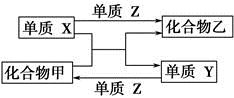
| 选项 | X | Y | Z | 甲 | 乙 |
| A | H2 | Si | Cl2 | SiCl4 | HCl |
| B | Mg | C | O2 | CO2 | MgO |
| C | Zn | Fe | Cl2 | FeCl2 | ZnCl2 |
| D | Cl2 | N2 | H2 | NH3 | HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系如图所示。则甲和X不可能是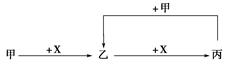
| A.甲为C,X为O2 |
| B.甲为SO2,X为NaOH溶液 |
| C.甲为Fe,X为Cl2 |
| D.甲为AlCl3溶液,X为NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
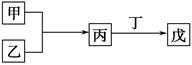
甲、乙、丙、丁、戊是中学化学常见的无机物,其中甲、乙均为单质,它们的转化关系如图所示(某些条件和部分产物已略去)。下列说法不正确的是
( )。
| A.若组成甲、乙的元素位于同一周期,则戊可能是一种弱酸 |
| B.若组成甲、乙的元素位于同一主族,则戊可能是一种弱酸 |
| C.若甲为短周期中原子半径最大的主族元素形成的单质,且戊为碱,则丙只能为Na2O2 |
| D.若丙、丁混合生成白烟,且丙为18电子分子,丁为10电子分子,则乙的水溶液可能具有漂白作用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com