
化学为人类基本的生存需要、进而追求生活乃至生命质量的提升提供了重要的保障。但某些人的贪得无厌和对化学原理的滥用败坏了化学学科声誉,我们每个人都应该避免成为这样的人。下列科学史上的重要发现与发明,从原理上看与化学学科没有直接相关性的是
A、1774年舍勒最早制得氯气,1820年前后漂白粉用于饮用水消毒
B、1869年门捷列夫发现元素周期律,使元素的性质更有规律可循
C、1902年哈伯开始对合成氨反应进行研究,工业化后提高了粮食产量
D、1942年费米进行了235U原子核裂变试验,从而开创原子能利用时代
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
A、B、C、D为四种可溶性盐,它们的阳离子分别是Ba2+、Ag+、Na+、
Cu2+中的某一种,阴离子分别是NO 、SO
、SO 、Cl-、CO
、Cl-、CO 中的某一种。(离子在物
中的某一种。(离子在物
质中不能重复出现)
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入足量盐酸,B盐的溶液有沉淀生成,D盐的溶液有
无色无味的气体逸出。
(1)根据①②实验事实可推断它们的化学式为A________,B________。
(2)写出足量盐酸与D反应的离子方程式 __________________________。
(3)写出C与Ba(OH)2溶液反应的离子方程式:
_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于放热反应H2+Cl2 2HCl,下列说法中,正确的是( )
2HCl,下列说法中,正确的是( )
A.产物所具有的总能量高于反应物所具有的总能量
B.反应物所具有的总能量高于产物所具有的总能量
C.断开1 mol H-H键和1 mol Cl-Cl键所吸收的总能量大于形成1mol H-Cl键所放出的能量
D.该反应中,化学能只转变为热能
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.金属单质在氧化还原反应中总是作还原剂
B.非金属单质在氧化还原反应中总是作氧化剂
C.钠原子在氧化还原反应中失去1个电子,而铝原子失去3个电子,所以铝比钠活泼,均能与氧气反应
D.金属在加热条件下均易和氧气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
往100 mL氢离子浓度为1mol·L-1的硫酸和硝酸混合液中投入3.84 g铜粉,微热使反应充分完成后,生成NO气体448 mL(标准状况)。则反应前的混合液中含硫酸的物质的量为
A. 0.01mol B. 0.02 mol C. 0.03 mol D. 0.04 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
焦炭是工业生产中的重要还原剂和燃料,活性炭用于生活和实验室中通过吸附作用除去有害气体或有毒物质。它们的化学成分都可以看成是碳单质。
(1)红热的焦炭投入浓硝酸中,写出反应的化学方程式 ;
(2)将一定条件下的高锰酸钾溶液与活性炭混合,可发生如下反应(未配平) MnO4-+ C+ H2O—— MnO2+ ① +CO32-,则 ① 处应该填入的微粒化学式为 ;
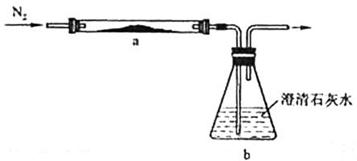 (3)PbO俗称密陀僧或铅黄,将黄色粉末状PbO和足量活性炭充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水,按图连接仪器。实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成。同时,b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续通氮气,直至反应管冷却。此时,管中的熔融物凝固成银白色金属。
(3)PbO俗称密陀僧或铅黄,将黄色粉末状PbO和足量活性炭充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水,按图连接仪器。实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成。同时,b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续通氮气,直至反应管冷却。此时,管中的熔融物凝固成银白色金属。
写出反应管a中发生的所有反应的化学方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
右图表示外界条件(温度、压强)的变化对下列反应的影响:L(s)+G(g)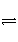
 2R(g) ΔH<0,在图中,Y轴是指( )
2R(g) ΔH<0,在图中,Y轴是指( )
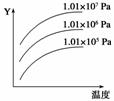
A.平衡混合气体中G的质量分数
B.平衡混合气体中R的质量分数
C.G的转化率
D.L的转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com