
| A、AgCl不溶于水,不能转化为AgI |
| B、一定温度下,向AgCl的饱和溶液中加入NaCl固体,有AgCl固体析出 |
| C、AgI比AgCl更难溶于水,所以AgCl可以转化为AgI |
| D、向AgCl沉淀的悬浊液中加入NaCl饱和溶液,AgCl的溶解度变小,溶度积常数变小 |


科目:高中化学 来源: 题型:

 (X表示卤素原子,下同).
(X表示卤素原子,下同).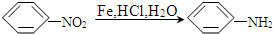
 互为同分异构体且苯环上有三个取代基的数目为
互为同分异构体且苯环上有三个取代基的数目为查看答案和解析>>
科目:高中化学 来源: 题型:
 的流程图.请回答下列问题:
的流程图.请回答下列问题:| 光照 |
| Cl2① |
| NaOH② |
| C2H5OH,△ |
| Br/CCl |
| ③ |
| NaOH④ |
| H2O,△ |
| O2⑤ |
| Cu,△ |
| 新制Cu((OH),H+ |
| △⑥ |
| ⑦H2 |
| 一定条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:

 生成Ⅳ的反应方程式为
生成Ⅳ的反应方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
 NOx是大气污染的主要污染物之一.
NOx是大气污染的主要污染物之一.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| A、Y元素的最高价氧化物对应水化物的化学式为H3YO4 |
| B、与等浓度的盐酸反应,Z单质比W单质更剧烈 |
| C、原子半径由小到大的顺序为X<Z<Y<W |
| D、Y的气态氢化物可与其最高价含氧酸反应生成共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 洋蓟属高档蔬菜,从洋蓟提取的物质A具有良好的保健功能和药用价值,A的结构如图.下列关于A的相关叙述正确的是( )
洋蓟属高档蔬菜,从洋蓟提取的物质A具有良好的保健功能和药用价值,A的结构如图.下列关于A的相关叙述正确的是( )| A、A在酸性条件下可以发生水解反应 |
| B、1mol A和足量NaOH溶液反应,最多消耗9mol NaOH |
| C、A能和浓溴水发生加成和取代反应 |
| D、A含4种官能团 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com