
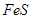 与一定浓度的
与一定浓度的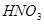 反应,生成
反应,生成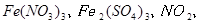
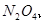
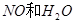 ,当
,当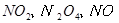 的物质的量之比为
的物质的量之比为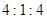 时,实际参加反应的
时,实际参加反应的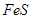 与
与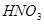 的物质的量之比为( )。
的物质的量之比为( )。| A.1:6 | B.2:15 | C.2:3 | D.16:25 |


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源:不详 题型:单选题
| A.2.20 | B.2.33 | C.2.00 | D.0.50 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应过程中,被氧化与被还原的元素的物质的量之比为2:1 |
| B.NF3是一种无色、无臭的气体,因此NF3在空气中泄漏时不易被察觉 |
| C.一旦NF3泄漏,可以用石灰水溶液喷淋的方法减少污染 |
| D.若反应中转移的电子数目为6.02×1023,生成22.4L NO气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NF3分子中所有原子共平面 | B.NF3在反应中既做氧化剂又做还原剂 |
| C.生成0.2mol HNO3时转移0.2mol电子 | D.氧化产物与还原产物的物质的量之比为2∶1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.18.0 L | B.27.0 L | C.31.4L | D.33.6 L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.制取NF3的反应中,氧化剂与还原剂的物质的量之比为1:3 |
| B.NF3在潮湿的空气中泄漏会产生红棕色气体 |
| C.若在制取NF3的反应中有2molNH3参加反应,转移电子的物质的量为12mol |
| D.它在潮湿的环境中NF3是氧化剂,H2O是还原剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.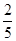 mol mol | B. mol mol | C. mol mol | D. mol mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1 :6 | B.6 :1 | C.1 :5 | D.5 :1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.7.5L | B.9.5L | C.13.6L | D.16.8L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com