
| A. | 溶液的导电性 | B. | 水的离子积 | C. | 离子总数 | D. | 溶液pH值 |
分析 酸碱中和反应中与温度 有关的物理量有弱电解质的电离平衡常数、水的离子积常数,
A.氢氧化钠溶液中加入少量稀醋酸发生反应生成醋酸钠和水,溶液导电性变化不大;
B.水的离子积常数随温度变化;
C.往NaOH溶液中加入少量的稀醋酸,发生中和反应生成醋酸钠完全电离氢氧根离子,碱性减弱水被抑制程度减弱;
D.氢氧化钠和醋酸反应生成醋酸钠,溶液中氢氧根离子浓度减小;
解答 解:A.氢氧化钠溶液中加入少量稀醋酸发生反应生成醋酸钠和水,溶液导电性变化不大,故A错误;
B.温度不变,水的离子积常数不变,故B错误;
C.往NaOH溶液中加入少量的稀醋酸,反应生成醋酸钠是强电解质,氢氧化钠中氢氧根离子物质的量减小和增大醋酸根离子物质的量相同,但碱性减弱水被抑制程度减弱,且加入稀醋酸溶液中加入了水,所以溶液中离子总数增大,故C正确;
D..往NaOH溶液中加入少量的稀醋酸,反应生成醋酸钠,溶液中氢氧根离子浓度减小,PH减小,故D错误;
故选C.
点评 本题考查了酸碱反应后溶液酸碱性、导电性、离子积常数、溶液PH等量的变化分析判断,掌握基础是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
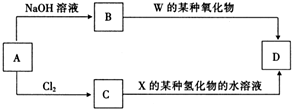
| W | X | ||
| Y | Z |
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
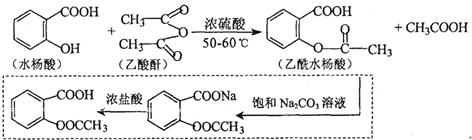
 .
. .
.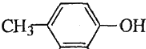 也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件:
也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件: .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe+CuSO4=FeSO4+Cu | B. | Cl2+H2O=HCl+HClO | ||
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | D. | AgNO3+HCl=AgCl↓+HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com