
����Һ����ʾ���Ĺ�����ʹ�õĻ�ѧ��ϴ��NF3�� һ���������壬��洢������������CO2��12000��20000�����ڴ����е������ɳ���740��֮�ã������Ǽ��ֻ�ѧ���ļ��ܣ�
һ���������壬��洢������������CO2��12000��20000�����ڴ����е������ɳ���740��֮�ã������Ǽ��ֻ�ѧ���ļ��ܣ�
��ѧ�� | N��N | F��F | N��F |
����/ kJ��mol��1 | 941.7 | 154.8 | 283.0 |
����˵������ȷ���ǣ� ��
A������N2(g)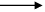 2N(g)�ų�����
2N(g)�ų�����
B������N(g)��3F(g)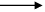 NF3(g)�ų�����
NF3(g)�ų�����
C����ӦN2(g)��3F2(g)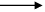 2NF3(g)�Ħ�H��0
2NF3(g)�Ħ�H��0
D��NF3�������������û�л�ѧ���Ķ��������ɣ����ܿ��ܷ�����ѧ��Ӧ
 �����ܿ����ϵ�д�
�����ܿ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�����ʡ������12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A.Ҫ��ȥCO2�л���������SO2�����ñ��͵�̼��������Һ
B.SO2��Cl2��Ϻ�����ˮƯ������ǿ
C.����������Ũ�����Ӧ���ʿ��ڳ�������������������Ũ����
D.��ʯ�Һ���ˮCaCl2���������ڸ���NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ɽ��ʡ�߶�12���¿���ѧ�Ծ��������棩 ���ͣ������
��.�����£���ijһԪ��HA(�ס��ҡ�������������ͬ��һԪ��)��NaOH��Һ�������ϣ�������Һ�����ʵ�����Ũ�Ⱥͻ��Һ��pH���±���ʾ��
ʵ���� | HA�����ʵ���Ũ��(mol��L-1) | NaOH�����ʵ���Ũ��(mol��L-1) | ��Ϻ���Һ��pH |
�� | 0.1 | 0.1 | pH��a |
�� | 0.12 | 0.1 | pH��7 |
�� | 0.2 | 0.1 | pH��7 |
�� | 0.1 | 0.1 | pH��10 |
��1���Ӽ����������������ж�HA��ǿ�ỹ��� ��
��2����������Һ������Ũ��c(A-)��c(Na+)�Ĵ�С��ϵ�� ��
A��ǰ�ߴ� B�����ߴ� C��������� D�����ж�
��3���ӱ���ʵ�����������û����Һ������Ũ���ɴ�С��˳���� ��
��4����������ʵ�����ݣ�д���û����Һ��������ʽ�ľ�ȷ���(��ʽ)��c(Na+)��c(A-)�� mol/L��
��.ij��Ԫ��(����ʽ��H2B��ʾ)��ˮ�еĵ��뷽��ʽ�ǣ�H2B=H++HB-��HB-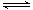 H++B2-
H++B2-
�ش��������⣺
��5����0.1 mol/L��Na2B��Һ�У���������Ũ�ȹ�ϵʽ��ȷ���� ��
A��c(B2-)+c(HB-)��0.1mol/L
B��c(B2-)+c(HB-)+c(H2B)��0.1mol/L
C��c(OH-)��c(H+)+c(HB-)
D��c(Na+)+c(OH-)��c(H+)+c(HB��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ɽ��ʡ�߶�12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����ˮ��Һһ�������Ե���
A��c(NH4+)=c(C1-)��NH4Cl ��Һ
B��c(H+)=1��10-7mol��L-1����Һ
C��pH=7����Һ
D�������½�pH=3������pH= 11�ļ�������Ϻ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���ຣʡ�߶�11���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���ڷ�ӦmA��nB==pC������˵����ȷ���ǣ� ��
A��ij�¶�ʱ����ѧ��Ӧ����������A��B��C�������ʱ�ʾ������ֵ����ͬ��
B�������������䣬����ѹǿ����Ӧ���ʼӿ�
C�������ӻ��СB�����ʵ�������Ӧ����һ���ᷢ�����Եı仯
D�������������䣬�����¶ȣ���Ӧ���ʼӿ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���ຣʡ�߶�11���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
25�桢101 kPa�£�1g����ȼ������Һ̬ˮ���ų�142.9kJ�������ܱ�ʾH2ȼ���ȵ��Ȼ�ѧ����ʽΪ( )
A��2H2(g)��O2(g) = 2H2O(1) ��H���D571.6kJ��mol
B��2H2(g)��O2(g) = 2H2O(1) ��H����571.6 kJ��mol
C��H2(g)�� O2(g) = H2O(g) ��H���D285.8 kJ��mol
O2(g) = H2O(g) ��H���D285.8 kJ��mol
D��H2(g)��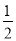 O2(g) = H2O(1) ��H���D285.8kJ��mol
O2(g) = H2O(1) ��H���D285.8kJ��mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ɹŸ�һ���л�ѧ���������棩 ���ͣ������
һ�������£�NO��NH3���Է�����Ӧ����N2��H2O��6NO+4NH3=5N2+6H2O������NO��NH3�Ļ����1mol����ַ�Ӧ�����ò����У�������ԭ�õ���N2�Ⱦ������õ���N2��1.4g��
��1���ڷ���ʽ�б������ת�Ƶķ������Ŀ��6NO+4NH3=5N2+6H2O��
��2�������Ϸ�Ӧ������ȫ���Լ���ԭ��Ӧ�������NO��NH3�����ʵ����ı�Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ɹŸ�һ���л�ѧ���������棩 ���ͣ�ѡ����
ͬ�¡�ͬѹ�£���ͬ����������X��Y����֪��ʱY���������X������������ǵ���Է���������ϵ��
A�� MX >MY B��MX <MY C��MX =MY D����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ӱ�ʡ�߶�11���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ������CO2����ͨ��2Lδ֪Ũ�ȵ�NaOH��Һ�У���������Һ����μ���ϡ�������� ����������Һ���ȣ�������������HC1�����ʵ����Ĺ�ϵ��ͼ��ʾ������������ܽ��HCl�Ļӷ�)������˵������ȷ���ǣ� ��
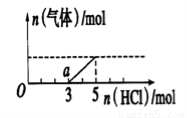
A��0����Һ���������ʵĻ�ѧʽΪNaOH��Na2CO3
B�������£�a����ҺpH>7
C����״���£�ͨ��CO2�����Ϊ4.48L
D��ԭNaOH��Һ�����ʵ���Ũ��Ϊ2.5mol/L
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com