
| A. | BF2Cl只有一种结构 | B. | 三根B-F键间键角都为120° | ||
| C. | BFCl2只有一种结构 | D. | 三根B-F键键长都为130pm |
分析 根据价电子对数判断其杂化类型,根据形成的杂化轨道判断其空间构型,BF3中B的价电子结构为2s22p1,形成了三条杂化轨道,B的杂化类型为sp2,三个sp2杂化轨道分别与三个F原子的p轨道成键,三根B-F键间键角都为120°,为平面三角形,BFCl2、BF2Cl只有一种结构,三根B-F键键长相等,也可能为三角锥型.
解答 解:A.BF2Cl只有一种结构,可能为三角锥型,不一定为平面三角形,故A错误;
B.BF3中B的价电子结构为2s22p1,价电子对数为:$\frac{3+3}{2}$=3,形成了三条杂化轨道,即B的杂化类型为sp2,形成3个共用电子对,无孤对电子,三个sp2杂化轨道分别与三个F原子的p轨道成键,三根B-F键间键角都为120°,为平面三角形,故B正确;
C.BFCl2只有一种结构,可能为三角锥型,不一定为平面三角形,故C错误;
D.三根B-F键键长都为130pm,可能为三角锥型中棱相等,不能说明BF3为平面三角形,故D错误;
故选B.
点评 本题主要以BF3的分子构型考查了杂化轨道理论的应用,题目难度不大,注意键长相等,也可能为三角锥型,为易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 ,分子的立体构型为V型,中心原子的杂化轨道类型为sp3杂化.
,分子的立体构型为V型,中心原子的杂化轨道类型为sp3杂化.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取样,进行焰色反应 | |
| B. | 取样,滴加酚酞试液 | |
| C. | 取样,加入足量稀HNO3,再滴加AgNO3溶液 | |
| D. | 取样,加入足量BaCl2溶液,再滴加紫色石蕊试液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
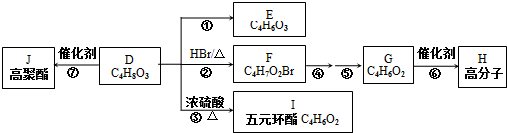
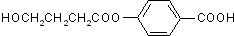 、I
、I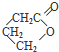 、J
、J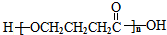 .
. .
. .
.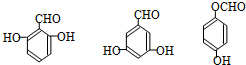 任意一种.
任意一种.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com