
【题目】实验室用下列溶质配制一种混合溶液,已知溶液中c(K+)=c(Cl﹣)= ![]() c(Na+)=c(SO
c(Na+)=c(SO ![]() ),则其溶质可能是( )
),则其溶质可能是( )
A.KCl、Na2SO4
B.KCl、Na2SO4、NaCl
C.NaCl、K2SO4
D.KCl、K2SO4、Na2SO4
【答案】A
【解析】解:A.当KCl、Na2SO4按照物质的量之比为1:1混合溶于水,得到溶液中离子浓度关系为:c(K+)=c(Cl﹣)= ![]() c(Na+)=c(SO
c(Na+)=c(SO ![]() ),故A正确; B.若满足c(K+)=c(Cl﹣),则不可能含有氯化钠,只有KCl、Na2SO4、NaCl都存在,则c(K+)<c(Cl﹣),故B错误;
),故A正确; B.若满足c(K+)=c(Cl﹣),则不可能含有氯化钠,只有KCl、Na2SO4、NaCl都存在,则c(K+)<c(Cl﹣),故B错误;
C.硫酸钾电离产生钾离子物质的量为硫酸根离子物质的量2倍,只含有NaCl、K2SO4 , c(K+)>c(SO ![]() ),故C错误;
),故C错误;
D.硫酸钠电离产生钠离子物质的量为硫酸根离子物质的量2倍,所以只有Na2SO4 , 满足 ![]() c(Na+)=c(SO
c(Na+)=c(SO ![]() ),再加K2SO4 , 则c(Na+)<2c(SO
),再加K2SO4 , 则c(Na+)<2c(SO ![]() ),故D错误;
),故D错误;
故选:A.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将物质的量均为0.1mol AlCl3、K2SO4和Al2(SO4)3溶于水,向其中加入一定量的Ba(OH)2溶液,测得溶液与沉淀中均含有铝元素,则生成BaSO4的物质的量不可能为( )
A.0.2mol
B.0.25 mol
C.0.35 mol
D.0.45 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学能与热能的说法正确的是
A. 铝热反应属于吸热反应
B. 若某反应的反应物的总能量大于生成物的总能量,则该反应为吸热反应
C. H2→H+H的变化需要吸收能量
D. 凡经加热而发生的化学反应都是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列有关反应的化学方程式,并注明有关反应条件:
(1)2-溴丙烷消去反应方程式________________________________;
(2)1,3-丁二烯的加聚反应方程式____________________________;
(3)CH3CH2CHO与新制Cu(OH)2反应的方程式_________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO是现代化工生产的基础原料,下列有关问题都和CO的使用有关。
(1)利用CO生产乙醇: 2CO(g)+4H2(g)![]() CH3CH2OH(g)+H2O(g)ΔH1
CH3CH2OH(g)+H2O(g)ΔH1
又已知:H2O(l)=H2O(g)ΔH2 CO(g)+H2O(g)![]() CO2(g)+H2(g)ΔH3
CO2(g)+H2(g)ΔH3
工业上也可利用CO2(g)与H2(g)为原料合成乙醇:
2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(l) ΔH
CH3CH2OH(g)+3H2O(l) ΔH
则:ΔH与ΔH1、ΔH2、ΔH3之间的关系是:ΔH=_______________________。
(2)一定条件下,H2、CO在体积固定的密闭容器中发生如下反应:4H2(g)+2CO(g)![]() CH3OCH3(g)+H2O(g)。下列措施中能够同时满足增大反应速率和提高CO转化率的是____(填字母)。
CH3OCH3(g)+H2O(g)。下列措施中能够同时满足增大反应速率和提高CO转化率的是____(填字母)。
A.使用高效催化剂 B.降低反应温度
C. 增大体系压强 D.不断将CH3OCH3从反应混合物中分离出来
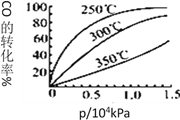
(3)采用CO与H2反应合成再生能源甲醇,反应如下:CO(g)+ 2H2(g)![]() CH3OH(g)。在一容积可变的密闭容器中充有10molCO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示。
CH3OH(g)。在一容积可变的密闭容器中充有10molCO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示。

①合成甲醇的反应为_______(填 “放热”或“吸热”)反应。
②A、B、C三点的平衡常数KA、KB、KC的大小关系为_____________。
③达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为_________L。
④CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示,实际生产时条件控制在250℃、1.3×104kPa左右,选择此压强的理由是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)已知:①CH3OH(l)+O2(g )= CO(g)+2H2O(g) △H= - 354.8 kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) △H= -566.0 kJ·mol-1
③H2O(g) = H2O(l) △H= -44.0 kJ·mol-1
请写出甲醇完全燃烧生成二氧化碳和液态水的热化学方程式:______________________________。
(2)某实验小组利用H2(g)、O2(g)、KOH(aq)设计成电池装置(装置Ⅰ),通过装置Ⅱ实现铁棒上镀铜。

①装置Ⅰ中,a口通入的气体为____________(填“H2”或“O2”),放电时,溶液中的K+向______极移动(填“正”或“负”),该电池负极的电极反应式为______________________。
②装置Ⅱ中,溶液c可选用________________溶液。
若电镀结束后,装置Ⅱ中Fe电极的质量改变了12.8g,则装置Ⅰ中理论上消耗氧气的体积为________L(标准状况下)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com