
【题目】已知下列热化学方程式:
①CaCO3(s)═CaO+CO2(g)△H=+177.7kJ
②C(s)+H2O(s)═CO(g)+H2(g)△H=﹣131.3kJmol﹣1
③ ![]() H2SO4(1)+NaOH(1)═
H2SO4(1)+NaOH(1)═ ![]() Na2SO4(1)+H2O(1)△H=﹣57.3kJmol﹣1
Na2SO4(1)+H2O(1)△H=﹣57.3kJmol﹣1
④C(s)+O2(g)═CO2(g)△H=﹣393.5kJmol﹣1
⑤CO(g)+ ![]() O2(g)═CO2(g)△H=﹣283kJmol﹣1
O2(g)═CO2(g)△H=﹣283kJmol﹣1
⑥HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(1)△H=﹣57.3kJmol﹣1
⑦2H2(g)+O2(g)═2H2O(1)△H=﹣517.6kJmol﹣1
(1)上述热化学方程式中,不正确的有 , 不正确的理由分别是 .
(2)根据上述信息,写出C转化为CO的热化学方程式: .
(3)上述反应中,表示燃烧热的热化学方程式有;表示中和热的热化学方程式有
【答案】
(1)①②③;①中CaO没标状态,△H单位应该为KJ/mol,②H2O的状态应为“g”,△H=+131.3KJ/mol,③除H2O外其它物质的状态不是“l”应为“aq”
(2)C(s)+ ![]() O2(g)=CO(g);△H=﹣110.5KJ/mol
O2(g)=CO(g);△H=﹣110.5KJ/mol
(3)④⑤;⑥
【解析】解:(1)根据热化学方程式的书写方法,①②③都是有错误的,错误之处分别是:①中CaO没标状态,△H单位应该为KJ/mol,②H2O的状态应为“g”,△H=+131.3KJ/mol,③除H2O外其它物质的状态不是“l”应为“aq”;
所以答案是:①②③;①中CaO没标状态,△H单位应该为KJ/mol,②H2O的状态应为“g”,△H=+131.3KJ/mol,③除H2O外其它物质的状态不是“l”应为“aq”;(2)结合化学反应④⑤,利用盖斯定律,反应C(s)+ ![]() O2(g)=CO(g)是④﹣⑤得来,所以焓变△H=﹣110.5KJ/mol,所以答案是:C(s)+
O2(g)=CO(g)是④﹣⑤得来,所以焓变△H=﹣110.5KJ/mol,所以答案是:C(s)+ ![]() O2(g)=CO(g);△H=﹣110.5KJ/mol;(3)上述反应中,④⑤分别是表示C、CO燃烧热的热化学方程式,⑥表示的是中和热的热化学方程式.
O2(g)=CO(g);△H=﹣110.5KJ/mol;(3)上述反应中,④⑤分别是表示C、CO燃烧热的热化学方程式,⑥表示的是中和热的热化学方程式.
所以答案是:④⑤;⑥.
【考点精析】本题主要考查了燃烧热和中和热的相关知识点,需要掌握在101kPa时1mol H2物质完全燃烧生成稳定的氧化物时所放出的能量,叫该物质的燃烧热;在稀溶液中,酸和碱发生中和反应而生成1mol H2O,这时的反应热叫做中和热才能正确解答此题.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】欲探究某矿石可能是由FeCO3、SiO2、Al2O3中的一种或几种组成,探究过程如图所示.(已知:碳酸不能溶解Al(OH)3沉淀) 
(1)用滤渣制备粗硅的化学反应方程式为
(2)下列说法正确的是
a.酸性:H2CO3>H2SiO3b.结合质子的能力:CO32﹣>AlO2﹣>HCO3﹣
c.稳定性:H2O>CH4>SiH4d.离子半径:O2﹣<Al3+
(3)滤渣和NaOH溶液反应的离子方程式是 , 通过现象说明此矿山中不含Al2O3
(4)该矿石和稀HNO3发生氧化还原反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向2L体积固定的密闭容器中加入1molHI,2HIH2(g)+I2(g)△H>0,H2的物质的量随时间的变化如图示,下列说法正确的是( ) 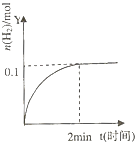
A.该温度下,反应的平衡常数是 ![]()
B.0~2min内的HI的平均反应速率为0.05mol?L﹣1?min﹣1
C.恒压下向该体系中加入N2 , 平衡不移动,反应速率不变
D.升高温度,平衡向正反应方向移动,只有正反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食品安全国家标准(GB2760﹣2014)规定葡萄酒中SO2最大使用量为0.25g/L.某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中SO2 , 并对SO2性质进行探究. 
(1)(i)仪器A的名称是;
(ii)仪器B中加入300mL葡萄酒和适量盐酸,加热使SO2全部逸出,并与C中H2O2完全反应,C中化学反应方程式为;
(2)小组同学为探究SO2的漂白性和还原性,设计了如下实验.
a漂白性 用如图2所示装置(气密性良好)进行实验,观察到如下现象:ⅰ中红色褪去、ⅱ中无变化.
(i)足量碱石灰的作用是;
(ii)从实验中可知使品红的水溶液褪色的微粒可能是;
b还原性 将SO2通入FeCl3溶液中,使其充分反应.
(iii)SO2与FeCl3反应的离子方程式是 , 如何检验该反应所得含氧酸根离子
(iv)实验中观察到溶液由黄色变为红棕色,静置一段时间,变为浅绿色.
已知:红棕色为FeSO3(墨绿色难溶物)与FeCl3溶液形成的混合色;Fe3+可氧化SO32﹣;则②中红棕色变为浅绿色的原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们会利用纳米级(1-100nm,1nm=10-9m)微粒物质制造出更加优秀的材料和器件,使化学在材料、能源、环境和生命科学等领域发挥越来越重要的作用。将纳米级微粒物质溶解于液体溶剂中形成一种分散系,对该分散系及分散质颗粒的叙述中正确的是( )
A. 该分散系能发生丁达尔效应 B. 该分散系为溶液
C. 该分散系属于悬浊液 D. 该分散系放置一段时间可能很快出现分层现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某一化学反应中,反应物A的浓度在3s内从1.0 mol/L变为0.4 mol/L ,在这3s内A的化学反应速率为
A. 1.8 mol/(L·s)B. 1.2 mol/(L·s)C. 0.6mol(L·s)D. 0.2 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某溶液中先滴加稀硝酸,再滴加氯化钡,有白色沉淀产生,该溶液
A. 一定含有SO42- B. 一定含有Ag+或SO42-
C. 一定含有SO32- D. 可能含有Ag+或SO42-或SO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】控制变量是科学研究的重要方法。相同质量的Fe与足量稀硫酸分别在下列条件下发生反应,其中化学反应速率最大的是
选项 | 硫酸浓度 | 反应温度 | 铁的状态 |
A. | 0.5 mol/L | 20℃ | 块状 |
B. | 0.5 mol/L | 20℃ | 粉末状 |
C. | 1 mol/L | 35℃ | 块状 |
D. | 2 mol/L | 35℃ | 粉末状 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂,实验室中可通过以下反应制得2KClO3+H2C2O4+H2SO4 ![]() 2ClO2↑+K2SO4+2CO2↑+2H2O.下列说法不正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O.下列说法不正确的是( )
A.KClO3发生还原反应
B.H2C2O4在反应中被氧化
C.H2C2O4的氧化性强于ClO2的氧化性
D.每生成1 mol ClO2 , 转移的电子数约为6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com