

 ��
������ B�IJ���������������һ�����ҵ�ʯ�ͻ���ˮƽ����BΪC2H4��ʯ�͵ķ���õ�ʯ���ͣ�ʯ�����ѽ�õ���ϩ����ϩ�����Ӿ۷�Ӧ����FΪ ����ϩ��ˮ�����ӳɷ�Ӧ����AΪCH3CH2OH���Ҵ���Cu��Ag�����������·���������Ӧ����CΪCH3CHO��CH3CHO�ɽ�һ����������DΪCH3COOH��CH3CH2OH��CH3COOH��Ũ���������·�Ӧ����������������EΪCH3COOCH2CH3����ϩ��HCl�����ӳɷ�Ӧ����HΪCH3CH2Cl���ݴ˽��
����ϩ��ˮ�����ӳɷ�Ӧ����AΪCH3CH2OH���Ҵ���Cu��Ag�����������·���������Ӧ����CΪCH3CHO��CH3CHO�ɽ�һ����������DΪCH3COOH��CH3CH2OH��CH3COOH��Ũ���������·�Ӧ����������������EΪCH3COOCH2CH3����ϩ��HCl�����ӳɷ�Ӧ����HΪCH3CH2Cl���ݴ˽��
��� �⣺B�IJ���������������һ�����ҵ�ʯ�ͻ���ˮƽ����BΪC2H4��ʯ�͵ķ���õ�ʯ���ͣ�ʯ�����ѽ�õ���ϩ����ϩ�����Ӿ۷�Ӧ����FΪ ����ϩ��ˮ�����ӳɷ�Ӧ����AΪCH3CH2OH���Ҵ���Cu��Ag�����������·���������Ӧ����CΪCH3CHO��CH3CHO�ɽ�һ����������DΪCH3COOH��CH3CH2OH��CH3COOH��Ũ���������·�Ӧ����������������EΪCH3COOCH2CH3����ϩ��HCl�����ӳɷ�Ӧ����HΪCH3CH2Cl��
����ϩ��ˮ�����ӳɷ�Ӧ����AΪCH3CH2OH���Ҵ���Cu��Ag�����������·���������Ӧ����CΪCH3CHO��CH3CHO�ɽ�һ����������DΪCH3COOH��CH3CH2OH��CH3COOH��Ũ���������·�Ӧ����������������EΪCH3COOCH2CH3����ϩ��HCl�����ӳɷ�Ӧ����HΪCH3CH2Cl��
��1����ҵ�ϣ���ʯ�ͻ��ʯ���͵ķ�����Ϊ��ʯ�͵ķ�����ʯ���ͻ��B�ķ�����Ϊ��ʯ�͵��ѽ⣬
�ʴ�Ϊ��ʯ�͵ķ���ʯ�͵��ѽ⣻
��2����AΪCH3CH2OH������������A�Ļ�ѧ���Ե�ԭ���ŵ�����Ϊ�ǻ����ʴ�Ϊ���ǻ���
��B��A�ķ�Ӧ����Ϊ���ӳɷ�Ӧ��A��E�ķ�Ӧ����Ϊ��������Ӧ���ʴ�Ϊ���ӳɷ�Ӧ��������Ӧ��
��C�ķ���ʽΪC2H4O��F�Ľṹ��ʽΪ ���ʴ�Ϊ��C2H4O��
���ʴ�Ϊ��C2H4O�� ��
��
��3����Ӧ�ڵĻ�ѧ����ʽΪ��2CH3CH2OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��
��Ӧ�ݵĻ�ѧ����ʽΪ��2CH3CH2OH+2Na��2CH3CH2ONa+H2����
�ʴ�Ϊ��2CH3CH2OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��2CH3CH2OH+2Na��2CH3CH2ONa+H2����
��4��������������������ȡ����Ӧ������Ӧ�࣬���ﲻ�������ʵͣ���ϩ���Ȼ����������Ǽӳɷ�Ӧ�����﴿�������ʸߣ��ʷ����������
�ʴ�Ϊ����������������������ȡ����Ӧ������Ӧ�࣬���ﲻ�������ʵͣ���ϩ���Ȼ����������Ǽӳɷ�Ӧ�����﴿�������ʸߣ�
���� ���⿼���л����ƶϣ��漰ϩ������ȩ������֮���ת����ϵ���ѶȲ���ע�����֪ʶ���������գ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | S2-+2H2O?H2S+2OH- | B�� | CH3COO-+H2O?CH3COOH+OH- | ||
| C�� | CH3COOH+H2O?CH3COO-+H3O+ | D�� | Fe3++3H2O?Fe��OH��3��+3H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
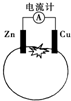
| A�� | һ��ʱ���пƬ��������� | B�� | ͭ�缫�����������ɫ | ||
| C�� | ������ͭͨ����������п | D�� | п�缫�Ǹõ�صĸ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ռ�ʱ������ʹ����ͨʯӢ������SiO2+2NaOH$\frac{\underline{\;\;��\;\;}}{\;}$Na2SiO3+H2O | |
| B�� | ��Na2SO3��NaI�Ļ����Һ�еμ�������ˮ��2I-+C12�T2 Cl-+I2 | |
| C�� | ���ȵ���˿��ˮ�Ӵ��������γ�����ɫ�����ɫ�������㣺3Fe+4H2O$\frac{\underline{\;\;��\;\;}}{\;}$Fe3O4+4H2 | |
| D�� | ��84����Һ������Ч�ɷ�NaClO���͡�����顱����Ҫ�ɷ�HCl�����ʹ�÷ų�������ClO-+Cl-+2H+�TCl2��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ijͬѧ�������ͼ��ʵ��װ�������Եزⶨ��ʯ��̼���Ƶ�����������
ijͬѧ�������ͼ��ʵ��װ�������Եزⶨ��ʯ��̼���Ƶ������������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | PAFC���ھ�������ˮʱ�����Գ�ȥˮ�����е��к����� | |
| B�� | PAFC������+2�� | |
| C�� | PAFC������������Һ | |
| D�� | PAFCû�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��X��Y����ͬһ���ڣ�����M�����������������ͷ��� | |
| B�� | ��X�ĵ��ʳ����������壬��Y�ĵ��ʳ�����Ҳ������ | |
| C�� | ��X��Y��Ԫ����������1�����������ӻ������Mֻ������ | |
| D�� | ��M�������ӻ���������п��ܺ��зǼ��Լ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������������ϡ���Fe3O4+8H+=Fe2++2Fe3++4H2O | |
| B�� | Ca��HCO3��2�����Ca��OH��2��Һ��Ӧ��Ca2++HCO3-+OH-=CaCO3��+H2O | |
| C�� | ������ͭ�����ϡ���2H++2Cl-$\frac{\underline{\;���\;}}{\;}$H2��+Cl2�� | |
| D�� | Na2S2O3��Һ�м���ϡ���2S2O+4H+�TSO42-+3S��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| Ԫ�� | A | B | C | D | E | F | G | H |
| ԭ�Ӱ뾶��nm�� | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 | 0.152 | 0.037 | 0.099 |
| ��Ҫ���ϼ� | +2 | +3 | +2 | +6��-2 | -2 | +1 | +1��-1 | +7��-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com