
| A. | SO2 | B. | H2 | C. | NH3 | D. | CO2 |
分析 浓硫酸具有酸性,能和碱性气体反应,浓硫酸具有强氧化性,能和强还原性气体反应,不能用浓硫酸干燥说明该气体和浓硫酸反应,据此分析解答.
解答 解:A.虽然浓硫酸具有强氧化性、二氧化硫具有还原性,但二者不能发生氧化还原反应,所以能用浓硫酸干燥二氧化硫,故A不选;
B.氢气和浓硫酸不反应,所以能用浓硫酸干燥氢气,故B不选;
C.氨气属于碱性气体,能和浓硫酸反应生成硫酸铵,所以不能用浓硫酸干燥氨气,故C选;
D.二氧化碳属于酸性气体,和浓硫酸不反应,所以能用浓硫酸干燥二氧化碳,故D不选;
故选C.
点评 本题考查气体的干燥,只要气体和干燥剂不反应的就能用该干燥剂干燥,熟悉常见干燥剂及气体的性质,注意浓硫酸不能干燥硫化氢、碘化氢等气体.


科目:高中化学 来源: 题型:解答题
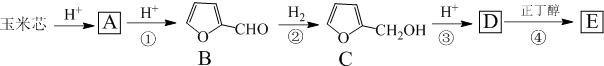
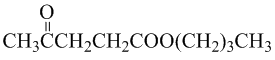 .
.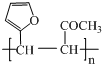 .写出反应的化学方程式
.写出反应的化学方程式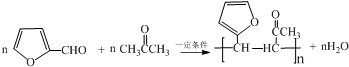 (不必注明反应条件).
(不必注明反应条件).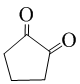 或
或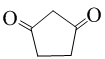 (任写一种).
(任写一种).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K2SO3已部分被空气中的氧气氧化 | |
| B. | 加入Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4 | |
| C. | 加硝酸后的不溶性沉淀中含有BaSO3 | |
| D. | 此实验不能确定K2SO3是否部分被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2既是氧化剂,又是还原剂 | |
| B. | NaNO2是氧化剂 | |
| C. | NH4Cl中的氮元素被还原 | |
| D. | 每生成1 mol N2时,转移电子的物质的量为6 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
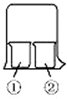 使用如图所示装置进行化学小实验,请填写下列空白:
使用如图所示装置进行化学小实验,请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mol | B. | 2mol | C. | 2.5mol | D. | 4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O和H2O2中的化学键类型完全相同 | |
| B. | N2的结构式为N-N | |
| C. | 一个D216O分子所含的中子数为10 | |
| D. | NaCl的电子式为 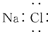 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com