
【题目】如图1,溶液A中可能含有Mg2+、Cu2+、Al3+、Fe2+四种阳离子,B为淡黄色固体,旋开E后,有气体放出和白色沉淀生成,淡黄色固体的物质的量与产生沉淀的质量关系如图2. 
(1)则溶液中含有的阳离子有 .
(2)写出图2曲线a~b段反应的离子方程式 , .
(3)A溶液中存在的阳离子的物质的量浓度之比为 .
【答案】
(1)Mg2+、Al3+
(2)2Na2O2+2H2O═4Na++4OH﹣+O2↑;Al(OH)3+OH﹣=AlO2﹣+2H2O
(3)1:2
【解析】解:(1)若溶液中有Cu2+会生成蓝色沉淀,有Fe3+会生成红褐色沉淀,题中只有白色沉淀,而且由图可知白色沉淀能部分溶于氢氧化钠,可知沉淀为氢氧化镁和氢氧化铝,所以溶液中的离子为:Mg2+、Al3+.所以答案是:Mg2+、Al3+;(2)横坐标为4﹣5moL时,发生的化学反应是:Na2O2先与水反应:2Na2O2+2H2O═4Na++4OH﹣+O2↑,生成的NaOH将Al(OH)3溶解:Al(OH)3+OH﹣=AlO2﹣+2H2O,
所以答案是:2Na2O2+2H2O═4Na++4OH﹣+O2↑;Al(OH)3+OH﹣=AlO2﹣+2H2O;(3)Al(OH)3完全溶解消耗消耗1moL过氧化钠即2molNaOH,由方程式可知n[Al(OH)3]=n(NaOH)=2mol,根据铝元素守恒可知,n(Al3+)=n[Al(OH)3]=2mol;
横坐标为0﹣4moL时发生的化学反应是:Mg2++2OH﹣=Mg(OH)2↓、Al3++3OH﹣=Al(OH)3↓沉淀为最大值时,该阶段消耗4mol过氧化钠即8molNaOH,根据OH﹣守恒,2n[Mg(OH)2]+3n[Al(OH)3]=n(NaOH),Mg2+物质的量为1mol,故Mg2+、Al3+的物质的量浓度之比为1:2,所以答案是:1:2.


科目:高中化学 来源: 题型:
【题目】某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如图所示。则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3的物质的量浓度之比为( )

A. 1∶1∶4
B. 1∶3∶1
C. 3∶3∶8
D. 1∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+。从工业废水中回收硫酸亚铁和金属铜的工艺流程如图所示。( )
下列说法正确的是
A.试剂X为铁粉
B.操作①为过滤;操作②为分液
C.溶液1和溶液2的溶质完全相同
D.试剂Y为硫酸铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(15分)凯氏定氨法是测定蛋白质中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐,然后通过滴定测量.已知:NH3+H3BO3=NH3H3BO3;NH3H3BO3+HCl=NH4Cl+H3BO3 . 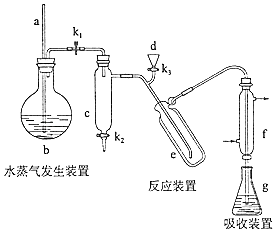
回答下列问题:
(1)a的作用是 .
(2)b中放入少量碎瓷片的目的是 . f的名称是 .
(3)清洗仪器:g中加蒸馏水:打开K1 , 关闭K2、K3 , 加热b,蒸气充满管路:停止加热,关闭K1 , g中蒸馏水倒吸进入c,原因是;打开K2放掉水,重复操作2~3次.
(4)仪器清洗后,g中加入硼酸(H3BO3)和指示剂,铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭K1 , d中保留少量水,打开K1 , 加热b,使水蒸气进入e.
①d中保留少量水的目的是 .
②e中主要反应的离子方程式为 , e采用中空双层玻璃瓶的作用是 .
(5)取某甘氨酸(C2H3NO2)样品m 克进行测定,滴定g中吸收液时消耗浓度为cmolL﹣1的盐酸V mL,则样品中氮的质量分数为%,样品的纯度≤%.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用固态不纯氯化钠(含少量NH4HCO3和Na2SO4杂质)制取纯净氯化钠溶液。下列操作可供选用:
①逐滴加入稀盐酸,调节pH值为5;
②煮沸;
③加蒸馏水溶解;
④加热至不再产生气体为止;
⑤加入稍过量的Na2CO3溶液;
⑥加入稍过量的BaCl2溶液;
⑦过滤。
上述实验操作的正确顺序应是
A.①②⑤⑥⑦③④ B.③④⑥⑤⑦①②
C.④③⑥⑤⑦①② D.④③⑤⑥⑦②①
【答案】C
【解析】
试题分析:NH4HCO3杂质可通过加热除去, Na2SO4杂质可通过BaCl2溶液除去,过量的BaCl2溶液可通过Na2CO3溶液除去,过量的Na2CO3溶液可通过滴加稀盐酸除去,答案选C。
考点:氯化钠的提纯
【题型】单选题
【结束】
22
【题目】设NA代表阿伏加德罗常数,下列说法正确的是
A. 常温下,5.6g铁与足量的盐酸反应,失去的电子数为0.2NA
B. 标准状况下11.2L二氧化硫中含有的原于数为2NA
C. 标准状况下,22.4L氯气发生反应转移电子数一定为2NA
D. 0.1mol/LCuCl2溶液中Cl-数目是0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒温恒容密闭容器中充入1mol CO2和3mol H2 , 一定条件下发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H=﹣49.0kJ/mol
测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.下列说法正确的是( )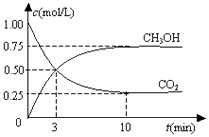
A.反应进行到3 min时,该反应达到平衡状态
B.从反应开始到平衡,CO2的转化率为25%
C.第3 min时,氢气的平均反应速率为1.5mol/(L?min)
D.该温度下,反应的平衡常数的值为 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】只给出表中甲和乙对应的量,不能用来求物质的量的是
甲 | 乙 | |
① | 物质微粒数 | 阿伏加德罗常数 |
② | 标准状况下气体摩尔体积 | 标准状况下气体体积 |
③ | 固体体积 | 固体密度 |
④ | 溶液质量分数 | 溶液体积 |
⑤ | 非标准状况下物质的质量 | 物质的摩尔质量 |
A. ②③④ B. ③④⑤ C. ③④ D. ④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com