
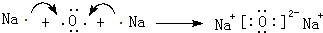 Ӣ
”¢ £®
£®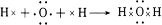 ”¢
”¢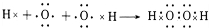 £®
£®·ÖĪö A”¢B”¢C”¢DĖÄÖÖŌŖĖŲ£¬Ē°ČżÖÖŌŖĖŲµÄĄė×Ó½į¹¹¶¼ŗĶÄŹŌ×Ó¾ßÓŠĻąĶ¬µÄŗĖĶāµē×ÓÅŲ¼£¬0.2molµÄCŌ×ÓÄÜ“ÓĖįÖŠÖĆ»»²śÉś2.24L H2£Ø±źæöĻĀ£©£¬ŌņZĪŖ½šŹō£¬Ęä»ÆŗĻ¼Ū=$\frac{\frac{2.24L}{22.4L/mol}”Į2}{0.2mol}$=1£¬æÉĶĘÖŖZĪŖNa£»DµÄŌ×ÓŗĖ֊ƻӊ֊×Ó£¬ŌņDĪŖHŌŖĖŲ£»AĆ»ÓŠÕż¼ŪĢ¬µÄ»ÆŗĻĪļ£¬BŗĶDæÉŠĪ³ÉµÄD2B·Ö×Ó£¬ŌņAĪŖFŌŖĖŲ”¢BĪŖOŌŖĖŲ£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗ£Ø1£©A”¢B”¢C”¢DĖÄÖÖŌŖĖŲ£¬Ē°ČżÖÖŌŖĖŲµÄĄė×Ó½į¹¹¶¼ŗĶÄŹŌ×Ó¾ßÓŠĻąĶ¬µÄŗĖĶāµē×ÓÅŲ¼£¬0.2molµÄCŌ×ÓÄÜ“ÓĖįÖŠÖĆ»»²śÉś2.24L H2£Ø±źæöĻĀ£©£¬ŌņZĪŖ½šŹō£¬Ęä»ÆŗĻ¼Ū=$\frac{\frac{2.24L}{22.4L/mol}”Į2}{0.2mol}$=1£¬æÉĶĘÖŖZĪŖNa£»DµÄŌ×ÓŗĖ֊ƻӊ֊×Ó£¬ŌņDĪŖHŌŖĖŲ£»AĆ»ÓŠÕż¼ŪĢ¬µÄ»ÆŗĻĪļ£¬BŗĶDæÉŠĪ³ÉµÄD2B·Ö×Ó£¬ŌņAĪŖFŌŖĖŲ”¢BĪŖOŌŖĖŲ£¬
¹Ź“š°øĪŖ£ŗ·ś£»Ńõ£»ÄĘ£»Ēā£»
£Ø2£©CÓėB»ÆŗĻµĆµ½ Na2O»ņÕß Na2O2£¬ÓƵē×ÓŹ½±ķŠĪ³É¹ż³Ģ£ŗ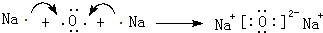 ”¢
”¢ £¬
£¬
BŗĶDæÉŠĪ³ÉµÄH2O»ņÕßH2O2£¬ÓƵē×ÓŹ½±ķŠĪ³É¹ż³Ģ£ŗ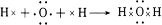 ”¢
Ӣ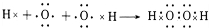
¹Ź“š°øĪŖ£ŗ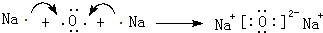 ”¢
”¢ £»
£»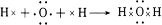 ”¢
”¢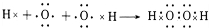 £»
£»
£Ø3£©CÓėBĖłŠĪ³ÉµÄ»ÆŗĻĪļĪŖNa2O»ņÕß Na2O2£¬DÓėBĖłŠĪ³ÉµÄ»ÆŗĻĪļĪŖĖ®£¬Ļą»„×÷ÓƵĥė×Ó·½³ĢŹ½£ŗNa2O+H2O=2Na++2OH-»ņ2Na2O2+2H2O=4Na++4OH-+O2”ü£¬
¹Ź“š°øĪŖ£ŗNa2O+H2O=2Na++2OH-»ņ2Na2O2+2H2O=4Na++4OH-+O2”ü£®
µćĘĄ ±¾Ģāæ¼²é½į¹¹ŠŌÖŹĪ»ÖĆ¹ŲĻµÓ¦ÓĆ£¬ĶʶĻŌŖĖŲŹĒ½āĢā¹Ų¼ü£¬²ąÖŲ¶Ō»ÆѧÓĆÓļµÄ漲飬עŅāÕĘĪÕµē×ÓŹ½±ķŹ¾»Æѧ¼ü»ņĪļÖŹµÄŠĪ³É£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øĆ»ÆŗĻĪļ½öŗ¬Ģ¼”¢ĒāĮ½ÖÖŌŖĖŲ | B£® | øĆ»ÆŗĻĪļÖŠĢ¼”¢ĒāŌ×ÓøöŹż±ČĪŖ1£ŗ2 | ||
| C£® | øĆÓŠ»śĪļµÄ·Ö×ÓŹ½ĪŖC2H6 | D£® | øĆ»ÆŗĻĪļÖŠŅ»¶Øŗ¬ÓŠŃõŌŖĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | -488.3 kJ•mol-1 | B£® | -191 kJ•mol-1 | ||
| C£® | -476.8 kJ•mol-1 | D£® | -1 549.6 kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā

| A£® | ·Ö×ÓŹ½ĪŖC3H2O3 | |
| B£® | ·Ö×ÓÖŠ¦Ņ¼üÓė¦Š¼üøöŹżÖ®±ČĪŖ3£ŗ1 | |
| C£® | ·Ö×ÓÖŠ¼ČÓŠ¼«ŠŌ¼üŅ²ÓŠ·Ē¼«ŠŌ¼ü | |
| D£® | ·Ö×ÓÖŠĢ¼Ō×ÓµÄŌӻƷ½Ź½Č«²æĪŖsp2ŌÓ»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | WX4ŹĒŅ»ÖÖÖŲŅŖµÄĒå½ąÄÜŌ“ | |
| B£® | ¹ĢĢ¬X2YŹĒ·Ö×Ó¾§Ģå | |
| C£® | ZWŹĒŌ×Ó¾§Ģ壬æÉÓĆ×÷ÄĶÄ„²ÄĮĻ | |
| D£® | ZY2µÄ¾§ĢåÖŠĆæøöZŌ×ÓÓėĮ½øöYŌ×ӳɼü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀĢÉ«»ÆѧµÄŗĖŠÄŹĒÓ¦ÓĆ»ÆѧŌĄķÖĪĄķ»·¾³ĪŪČ¾ | |
| B£® | æÉČÜŠŌĶŃĪÓŠ¶¾£¬µ«ŌŚÉśĆüĢåÖŠ£¬ĶŹĒŅ»ÖÖ²»æÉȱɣµÄĪ¢ĮæŌŖĖŲ | |
| C£® | »Æױʷ֊µÄ”°ĢģČ»Ö²Īļ¾«»Ŗ”±ŌŚĢįČ”¹ż³ĢÖŠæÉÄÜÓƵ½»Æѧ֊µÄŻĶČ””¢ÕōĮó¼¼Źõ | |
| D£® | ±½ŹĒÖŲŅŖ»Æ¹¤ŌĮĻ£¬±»Ó¢¹śæĘѧ¼Ņ·ØĄµŚŹ×ĻČ·¢ĻÖ£¬ŅŌĆŗŗĶŹÆÓĶĪŖŌĮĻĶعż»Æѧ±ä»Æ¾łæɵƵ½±½ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
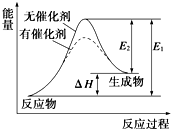 ij·“Ó¦µÄ·“Ó¦¹ż³ĢÖŠÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£ØĶ¼ÖŠE1±ķŹ¾Õż·“Ó¦µÄ»ī»ÆÄÜ£¬E2±ķŹ¾Äę·“Ó¦µÄ»ī»ÆÄÜ£©£®ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ£Ø””””£©
ij·“Ó¦µÄ·“Ó¦¹ż³ĢÖŠÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£ØĶ¼ÖŠE1±ķŹ¾Õż·“Ó¦µÄ»ī»ÆÄÜ£¬E2±ķŹ¾Äę·“Ó¦µÄ»ī»ÆÄÜ£©£®ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ£Ø””””£©| A£® | øĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦ | |
| B£® | øĆ·“Ó¦µÄ·“Ó¦ČȵČÓŚE1-E2 | |
| C£® | “߻ƼĮÄÜøıäøĆ·“Ó¦µÄģŹ±ä | |
| D£® | Äę·“Ó¦µÄ»ī»ÆÄÜ“óÓŚÕż·“Ó¦µÄ»ī»ÆÄÜ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā


²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com