
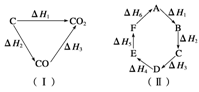
| A.A―→F ΔH=-ΔH6 |
| B.A―→D ΔH=ΔH1+ΔH2+ΔH3 |
| C.ΔH1+ΔH2+ΔH3+ΔH4+ΔH5+ΔH6=0 |
| D.ΔH1+ΔH6=ΔH2+ΔH3+ΔH4+ΔH5 |
科目:高中化学 来源:不详 题型:单选题
 2SO3(g);ΔH=-197 kJ·mol-1,当达到化学平衡时,下列说法中正确的是( )
2SO3(g);ΔH=-197 kJ·mol-1,当达到化学平衡时,下列说法中正确的是( )| A.生成SO3 2 mol | B.含氧原子共8 mol |
| C.放出197 kJ热量 | D.SO2和SO3共2 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


| A.负极的电极反应式为: CO+O2—―2e-=CO2 |
| B.工作时电极b作正极,O2-由电极a流向电极b |
| C.工作时电子由电极a通过传感器流向电极b |
| D.传感器中通过的电流越大,尾气中CO的含量越高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3 (g) △H =-196.6kJ·mol-1
2SO3 (g) △H =-196.6kJ·mol-1 2NO2 (g) △H =-113.0kJ·mol-1
2NO2 (g) △H =-113.0kJ·mol-1 SO3 (g) +NO(g)的△H =______kJ·mol-1
SO3 (g) +NO(g)的△H =______kJ·mol-1 CH3OH (g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H _____0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,
CH3OH (g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H _____0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.22 mol | B.0.15 mol |
| C.0.1 mol | D.0.05 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.+488.3kJ/mol | B.—488.3 kJ/mol |
| C.—244.15 kJ/mol | D.+244.15 kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
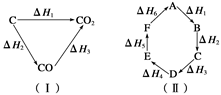
| A.ΔH1+ΔH6=ΔH2+ΔH3+ΔH4+ΔH5 |
| B.A―→D ΔH=ΔH1+ΔH2+ΔH3 |
| C.A―→F ΔH=-ΔH6 |
| D.ΔH1+ΔH2+ΔH3+ΔH4+ΔH5+ΔH6=0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 稀溶液发生中和反应的中和热为57.3 kJ/mol,辛烷的燃烧热为5518 kJ/mol。下列热化学方程式书写正确的是( )
稀溶液发生中和反应的中和热为57.3 kJ/mol,辛烷的燃烧热为5518 kJ/mol。下列热化学方程式书写正确的是( )| A.2H+(aq) +SO42-(aq)+Ba2+(aq)+2OH-(aq)=BaSO4(s)+2H2O(1);ΔH=-57.3 kJ/mol |
B.KOH(aq )+ )+ H2 SO4(aq)=K2SO4(aq)+H2O(l);ΔH=-57.3kJ/mol H2 SO4(aq)=K2SO4(aq)+H2O(l);ΔH=-57.3kJ/mol |
| C.2C8H18(g)+25O2(g)=16CO2(g)+18H2O(1);ΔH=-5518 kJ/mol |
| D.C8H18(l)+ 25/2 O2(g)=8CO2(g)+ 9H2O(1);ΔH=-5518 kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.488.3 kJ·mol-1 | B.-244.15 kJ·mol-1 |
| C.244.15 kJ·mol-1 | D.-488.3 kJ·mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com